
【题目】如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)过程中的能量变化示意图,已知E1=xkJmol﹣1、E2=ykJmol﹣1, 下列有关说法中正确的是( )
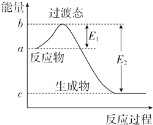
A.反应的活化能等于ykJmol﹣1
B.若对反应体系加热,△H不变
C.若在反应体系中加入催化剂,E1不变
D.1 molSO2Cl2(g)和1molSCl2(l)反应生成SOCl2(g)的△H=(x﹣y)kJmol﹣1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某化学教师为 “氯气与金属钠反应”设计了如图装置的实验。实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述中错误的是( )

A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 发生的反应为2Na+Cl2![]() 2NaCl
2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含 70%Cu、25%Al、4%Fe 及少量 Au、Pt 的合金,并设计出由合金制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1)第①步 Cu与酸反应的离子方程式为__________________,得到滤渣 1的主要成分为_______________。
(2)第②步加 H2O2的作用是做氧化剂,将溶液中的 Fe2+氧化为 Fe3+,用 H2O2做氧化剂的优点是____________________。
(3)滤渣 2的主要成分是 Al(OH)3和 Fe(OH)3,在生产中如何分离两种沉淀,写出反应的离子方程式______________。
(4)第③步蒸发所需玻璃仪器为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式______。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式______。
(3)酸雨是指pH<_____的降水。大量燃烧含硫煤产生气体随雨水降落到地面,随时间变长雨水酸性会逐渐增强,试用化学方程式解释其原因_________。在煤中加入适量石灰石,可以大大减少煤燃烧时SO2的排放,同时得到硫酸钙,发生反应的化学方程式__________。
(4)空气质量报告的各项指标可以反映出各地空气的质量,下列气体已纳入我国空气质量报告的是______(填字母)。
A.CO2 B.N2 C.NO2 D.O2
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与金属铜发生反应的离子方程式___________。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_______。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。用0.1 mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法正确的是( )
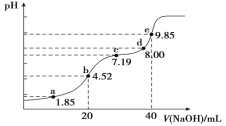
A.a点所得溶液中:2c(HSO3-)+c(SO32-)=0.1 mol/L
B.b点所得溶液中:c(H+)+c(SO32-)=c(OH-)+c(H2SO3)
C.c点所得溶液中:c(Na+)>3c(HSO3-)
D.d点所得溶液中:c(Na+)>c(OH-) >c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正在研制的一种“高容量、低成本”锂——铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )
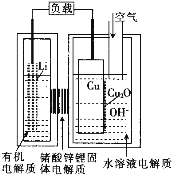
A.通空气时,铜被腐蚀,表面产生CuO
B.放电一段时间后右侧水溶液电解质中LiOH浓度逐渐增大
C.放电时,正极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH-
D.整个反应过程中,铜相当于催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的乙醇电池,它用磺酸类质子溶剂。电池总反应为:C2H5OH +3O2→ 2CO2+3H2O,电池示意如图,下列说法正确的是

A. a极为电池的正极
B. 电池工作时电流由a极沿导线经灯泡再到b极
C. 电池负极的电极反应为:4H++ O2+ 4e-= 2H2O
D. 电池工作时,1mol乙醇被氧化时就有12mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量铜和适量的浓硝酸反应,随着反应的进行,所生成的气体颜色逐渐变浅,当铜反应完毕后,共收集到11.2L由NO和NO2组成的混合气体(标准状况),将该气体与0.325molO2混合溶于水,恰好无气体剩余。则反应中消耗硝酸的物质的量为( )
A.1.2molB.1.1molC.1.8molD.1.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化:
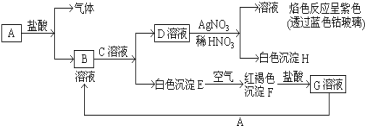
(1)写出下列各物质的化学式:
A___,B____,D___,F___,G___。
(2)写出由E转变成F的化学方程式___。
鉴别溶液G的试剂是__,现象___。
(3)G溶液和A反应的离子方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com