
【题目】已知有以下物质相互转化:
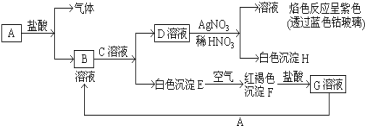
(1)写出下列各物质的化学式:
A___,B____,D___,F___,G___。
(2)写出由E转变成F的化学方程式___。
鉴别溶液G的试剂是__,现象___。
(3)G溶液和A反应的离子方程式:___。
【答案】Fe FeCl2 KCl Fe(OH)3 FeCl3 4Fe(OH)2+2H2O+O2=4Fe(OH)3 KSCN溶液 溶液变红色 2Fe3++Fe=3Fe2+
【解析】
D和硝酸银溶液反应生成白色沉淀H,H不溶于稀硝酸,所以H是氯化银,则D中含有氯离子,D和硝酸银混合溶液进行焰色反应呈紫色,则D中含有钾元素,所以D是氯化钾,白色沉淀E和氧气反应生成红褐色沉淀F,则F是氢氧化铁,E是氢氧化亚铁,氢氧化铁和盐酸反应生成氯化铁溶液,所以G是氯化铁,氯化铁和A反应生成B,B和C反应生成氯化钾和氢氧化亚铁,所以A是铁,B是氯化亚铁,C是氢氧化钾,据此分析解答。
(1)根据上述分析,A是铁,B是氯化亚铁,C是氢氧化钾,D是氯化钾,E是氢氧化亚铁,F是氢氧化铁,G是氯化铁,H是氯化银,故答案为:Fe;FeCl2;KCl; Fe(OH)3;FeCl3;
(2)氢氧化亚铁很容易被氧气氧化为氢氧化铁,反应的化学方程式为:4Fe(OH)2+2H2O+O2═4Fe(OH)3 ,鉴别FeCl3溶液,可以选KSCN溶液,若变为血红色,说明溶液中含有铁离子,故答案为:4Fe(OH)2+2H2O+O2═4Fe(OH)3;KSCN溶液;溶液变为血红色;
(3)铁和三价铁反应生成亚铁离子,反应的离子方程式为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+。


科目:高中化学 来源: 题型:
【题目】如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)过程中的能量变化示意图,已知E1=xkJmol﹣1、E2=ykJmol﹣1, 下列有关说法中正确的是( )
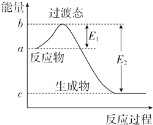
A.反应的活化能等于ykJmol﹣1
B.若对反应体系加热,△H不变
C.若在反应体系中加入催化剂,E1不变
D.1 molSO2Cl2(g)和1molSCl2(l)反应生成SOCl2(g)的△H=(x﹣y)kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A(g)和2 mol B(g)在2 L的恒容密闭容器中混合并在一定条件下发生反应:2A(g)+B(g) 2C(g) ΔH<0,反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是
A.2 s后物质A的转化率为70%
B.当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态
C.达到平衡状态时,增加A的物质的量,A和B的转化率都提高
D.达到平衡状态时,升高温度,平衡逆向移动,同时化学平衡常数K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是____________________。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:______________________。
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是____;
②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得21.525g白色沉淀。则溶液中c(Cl-)=___mol·L-1。
③验证该溶液中含有Fe2+,正确的实验方法是_________________。
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
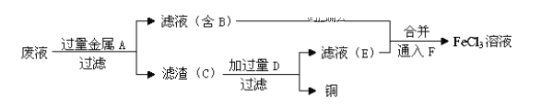
①滤渣C的化学式为___________。
②加过量D发生反应的离子方程式为_________________________。
③通入F发生反应的化学方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色。
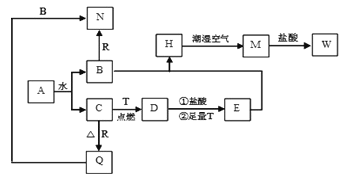
(1)写出下列物质的化学式:A:_____;E:______。
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:_______。
(3)按要求写方程式:B和R反应生成N的离子方程式:____________;M→W的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2 =2AB的能量变化如图所示。下列说法正确的是( )
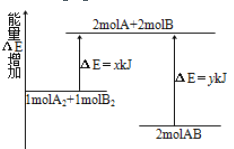
A. 该反应是吸热反应
B. 2 mol A—B键断裂需要吸收y kJ 的能量
C. 1 mol A—A键和1mol B—B键断裂能放出x kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,H2和CO的混合气体共8.96L,测得其质量为6.0g。计算此混合气体中:
(1)H2和CO的物质的量各为多少?_____________
(2)标准状况下,H2和CO的体积各为多少?_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下分别向20.00 mL 0.1000 mol·L-1的氨水、醋酸铵溶液中滴加0.1000mol·L-1的盐酸,溶液pH与加入盐酸体积的变化关系如图所示。下列说法正确的是

A. M点溶液中c (OH-)>c(NH4+)>c(NH3·H2O)>c(H+)
B. N点溶液中c(NH4+)>c(NH3·H2O)>c(Cl-)>c(OH-)
C. P点溶液中c(NH4+)>2c(CH3COO-)+c(NH3·H2O)
D. Q点溶液中2c(Cl-)>c(CH3COOH)+c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置或操作进行的相应实验,能达到实验目的的是

A. 用图甲所示装置分离乙醇和碘的混合液
B. 用图乙所示操作配制100 mL 0.1 mol·L-1硫酸溶液
C. 用图丙所示装置制备氨气
D. 用图丁所示装置检验浓硫酸与蔗糖反应产生的二氧化硫
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com