
����Ŀ����ˮ�������õIJ��ֹ�������ͼ��ʾ��

(1)������һ�������ȿ�����ˮ�������������壬����SO2��ˮ��Һ���仹ԭ���գ�������Ӧ�Ļ�ѧ����ʽΪ_____________________��
(2)Ϊ��ʹMg2+ת��ΪMg(OH)2���Լ��ٿ�����_________________(�ѧʽ)
(3)��ˮMgCl2������״̬�£�ͨ�������Mg��Cl2���÷�Ӧ�Ļ�ѧ����ʽΪ_______��
(4)�����йغ�ˮ�ۺ����õ�˵���������_____(����ĸ����)��
A.���οɲ��ó��Ӻͽᾧ�ȹ����ᴿ B.��ⱥ��ʳ��ˮ���Ƶý�����
C.����Һ��ͨ��C12��Ϊ������Br- D.��ˮ��þ�������漰���ֽⷴӦ
���𰸡�Br2 + SO2 + 2H2O =2HBr + H2SO4 Ca(OH)2  B
B
��������
(1)������Ӧ�Ļ�ѧ����ʽΪBr2 + SO2 + 2H2O =2HBr + H2SO4��
(2)Ϊ��ʹMg2+ת��ΪMg(OH)2���Լ��ٿ�����CaO�� Ca(OH)2��
(3)��Ӧ�Ļ�ѧ����ʽΪ
(4) A.�����к���Ca2+��Mg2+��SO42-�����ʣ�����ʱͨ������Һ�������м��������BaCl2��Һ��������NaOH��Һ������Na2CO3��Һ�����˺�����Һ�м�����������Һ�����ԣ��ٽ����ؽᾧ�����ᴿ����A��ȷ��
B.��ⱥ��ʳ��ˮ���ɵ����������������������ƣ���������Ȼ��������ƺ���������B����
C. ����Һ��ͨ��C12��Ϊ������Br-���������ӷ�ӦΪCl2 + 2Br- = 2Cl- + Br2�������壬��C��ȷ��
D.��ˮ��þ���̣��漰����������þ��������þ�����ᷴӦ�����Ȼ�þ����������Ȼ�þ������þ����������������þCa(OH)2+MgCl2=Mg(OH)2��+CaCl2��������þ�����ᷴӦ�����Ȼ�þMg(OH)2+2HCl= MgCl2+H2O��Ϊ���ֽⷴӦ����D��ȷ��
�ʴ�Ϊ��B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(8��)��¯���������з�������Ҫ��ӦΪ
![]()
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�

��ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK=_____________����H________0(����>������<������=��)��
(2)��һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0 mol����Ӧ����l0 min��ﵽƽ�⡣���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ������(C02)= _____________��CO��ƽ��ת����= _____________��
(3)�����(2)��CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_____________��
A������Fe���� | B������Fe203���� | C���Ƴ�����C02 |
D����߷�Ӧ�¶� E����С�������ݻ� F��������ʵĴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƻ������ӵĽṹ��ʽΪ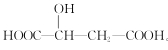 ������˵����ȷ����
������˵����ȷ����
A. 1molƻ��������������Na��Ӧ����1mol H2
B. 1molƻ�������3mol NaOH������Ӧ
C. ƻ��������еĹ��������ǻ����Ȼ�
D. ![]() ��ƻ���ụΪͬ���칹��
��ƻ���ụΪͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2017������)��ѹ���ʻ�������������ԭ��Ϊ��Ni(s)+4CO(g)![]() Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
�ڶ��Σ�����һ�η�Ӧ���������������������230���Ƶøߴ�����
�����ж���ȷ����
A. ����c(CO)��ƽ���������ƶ�����Ӧ��ƽ�ⳣ������
B. �ڶ��Σ�Ni(CO)4�ֽ��ʽϵ�
C. ��һ�Σ���30����50������֮��ѡ��Ӧ�¶ȣ�ѡ50��
D. �÷�Ӧ�ﵽƽ��ʱ��v����[Ni(CO)4]=4v����(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ҫ��������������ʵ�ֵ��ǣ���������
A.H2SO4��H2B.Fe2+��Fe3+C.O2��H2OD.HNO3��NO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�[��ѧ����ѡ��5���л���ѧ����]
�����б��������������E�뻯����H��Cr-Ni���¿��Է���ż����Ӧ���ϳ�һ�ֶ�����ŵĻ�����Y����ϳ�·�����£�

��֪��![]()
�ش��������⣺
��1��A�Ļ�ѧ������________________��
��2��BΪ���ȴ�������B����C�Ļ�ѧ����ʽΪ________________��
��3����A����B��G����H�ķ�Ӧ���ͷֱ���________________��________________��
��4��D�Ľṹ��ʽΪ________________��
��5��Y�к��������ŵ�����Ϊ________________��
��6��E��F��Cr-Ni����Ҳ���Է���ż����Ӧ������Ľṹ��ʽΪ________________��
��7��X��D��Ϊͬ���칹�壬�Ҿ�����ȫ��ͬ�����š�X�ĺ˴Ź���������ʾ���ֲ�ͬ��ѧ�������⣬������֮��Ϊ3��3��2��д��3�ַ�������������X�Ľṹ��ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.�ǽ���������һ�����ڹ��ۼ�
B.�����ۼ��Ļ�����һ���ǹ��ۻ�����
C.�����Ӽ��Ļ�����һ�������ӻ�����
D.����ˮ�ܵ���Ļ�����������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ��Ϊ�ʱ���ر䶼�뷴Ӧ���Է����й�,����ʱ���ر�����Ե�����Ϊ��Ӧ�Է��Ե��о�
B. 25 �桢101 kPaʱ,1 mol S��2 mol S��ȼ���Ȳ����
C. ͨ�����ǰѲ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ���
��ѧ�� | H��H | Cl��Cl | H��Cl |
����1 mol��ѧ ��ʱ�ų������� | 436 kJ��mol-1 | 243 kJ��mol-1 | 431 kJ��mol-1 |
��1/2H2(g)+ 1/2Cl2(g)![]() HCl(g)����H=-183 kJ��mol-1
HCl(g)����H=-183 kJ��mol-1
D. �κλ�ѧ��Ӧ�������������ı仯
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com