
【题目】下列说法中正确的是
A. 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
B. 25 ℃、101 kPa时,1 mol S和2 mol S的燃烧热不相等
C. 通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能
化学键 | H—H | Cl—Cl | H—Cl |
生成1 mol化学 键时放出的能量 | 436 kJ·mol-1 | 243 kJ·mol-1 | 431 kJ·mol-1 |
则1/2H2(g)+ 1/2Cl2(g)![]() HCl(g) ΔH=-183 kJ·mol-1
HCl(g) ΔH=-183 kJ·mol-1
D. 任何化学反应都伴随着能量的变化
【答案】D
【解析】
反应能否自发进行,取决于焓变和熵变的综合判据;燃烧热不随物质的量的变化而变化;反应热=反应物的总键能-生成物的总键能;化学反应的实质是旧键断裂,新键形成,断裂旧键要吸收能量,形成新键要放出能量。
反应能否自发进行,取决于焓变和熵变的综合判据,不能用焓变或熵变均可以单独作为反应自发性的判据,A错误;燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,燃烧热与反应物的多少无关,所以1mol S和2mol S的燃烧热相等,B错误;由反应热=反应物的总键能-生成物的总键能=436kJ/mol+243kJ/mol-431kJ/mol×2=-183.0kJ/mol,所以H2(g)+Cl2(g)═2HCl(g)△H=-183 kJmol-1,C错误;化学反应的实质是旧键断裂,新键形成,断裂旧键要吸收能量,形成新键要放出能量,所以任何化学反应都伴随着能量变化,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如下图所示。

(1)富集溴一般先用热空气或水蒸气吹出单质溴,再用SO2的水溶液将其还原吸收,发生反应的化学方程式为_____________________。
(2)为了使Mg2+转化为Mg(OH)2,试剂①可以用_________________(填化学式)
(3)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为_______。
(4)下列有关海水综合利用的说法错误的是_____(填字母代号)。
A.粗盐可采用除杂和结晶等过程提纯 B.电解饱和食盐水可制得金属钠
C.向滤液中通入C12是为了氧化Br- D.海水提镁过程中涉及复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】知识的梳理和感悟是有效学习的方法之一。某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
(1)图中,电解一段时间后,气球b中的气体是________(填化学式),U形管________(填“左”或“右”)边的溶液变红。

(2)利用图制作一种环保型消毒液发生器,可制备“84”消毒液的有效成分,则c为电源的________极;该发生器中反应的总离子方程式为_______________________________。

(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
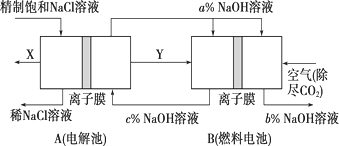
①燃料电池B中的电极反应式分别为
负极:_______________________________________________________,
正极:_______________________________________________________。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 可以写成
可以写成![]() 。有机物A的结构如下图所示,请回答:
。有机物A的结构如下图所示,请回答:

(1)有机物A分子所含官能团的名称为__________________。
(2)1mol A最多与____mol H2在一定条件下反应可生成环烃B。
(3)有机物A的分子式为_____________________________。
(4)有机物C是A的同分异构体,属于芳香烃,且C在一定条件下可发生聚合反应,生成高分子化合物D。则C的结构简式为______________,D的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向HCl、NH4Cl、AlCl3溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)随加入NaOH溶液体积(V)的关系正确的是( )
A. 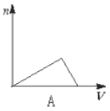 B.
B. 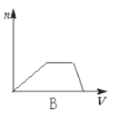
C. 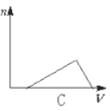 D.
D. 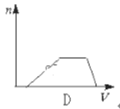
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。其中X、Y、Z都为气体,反应在t1min时到达平衡,如图所示,下列说法正确的是( )

A. 该反应的化学方程式是2X=3Y+Z
B. 已知1molX完全反应要吸收46kJ的热量,则至t1min时,该反应吸收的热量为36.8kJ·mol-1
C. 在此t1min时间内,用Y表示反应的平均速率v(Y)为0.6mol/(L·min)
D. 在相同状态下,反应前的压强是反应后的0.75倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,能说明反应A(s)+ 2B(g)![]() C(g)+ D(g)一定处于化学平衡状态的是
C(g)+ D(g)一定处于化学平衡状态的是
A. 混合气体的密度不再改变 B. 容器内的压强保持不变
C. C与D的物质的量相等 D. 消耗1 mol B的同时生成 0.5 mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体为b L(标况)。反应的离子方程式为_______________,样品中铝的物质的量为_____________(用含b的代数式表示)。
(2)若取a g样品,在高温下能恰好完全反应,该反应的化学方程式为________________,样品中氧化铁与铝的质量比为_________________(用含a 、b的代数式表示)。
(3)待(2)中反应产物冷却后,往其中加入足量的盐酸,测得生成的气体体积为c L(标况),则该气体与(1)中所得的气体的体积比c∶b=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅元素有质量数为28、29、30三种同位素,硅元素的近似相对原子质量为28.1,自然界中质量数为28的硅原子百分含量为92%,则质量分数为29、30的原子个数比为
A.3:5B.3:1C.2:3D.3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com