
【题目】有机高分子化合物甲是一种常用的光敏高分子材料,其结构简式为:
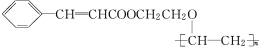
按下图流程可以合成甲,其中试剂Ⅰ可由相对分子质量为26的烃与水加成制得。
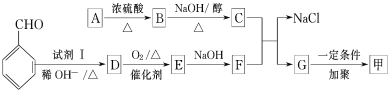
已知:
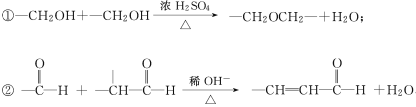
回答下列问题:
(1)质谱图显示A的相对分子质量是80.5。A分子中氧元素的质量分数为19.88%,碳元素的质量分数为29.81%,其余为氢元素和氯元素。A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2∶2∶1。A的结构简式为 。
(2)试剂Ⅰ的名称是________________;B→C的反应类型是________________。
(3)写出下列反应的化学方程式:
①A→B:________________________;
②D→E:________________________;
③C与F的反应:________________________。
(4)E的一种同分异构体,水解产物有两种,一种能使溴水褪色,另一种在滴加饱和溴水后,有白色沉淀生成,该物质的结构简式为 。
【答案】(1)ClCH2CH2OH;
(2)乙醛;消去;
(3)①2ClCH2CH2OH ![]() ClCH2CH2OCH2CH2Cl+H2O
ClCH2CH2OCH2CH2Cl+H2O
②2![]() +O2
+O2![]() 2
2![]() +H2O;
+H2O;
③![]() +
+![]()
![]()
![]() +NaCl;
+NaCl;
(4)![]()
【解析】
试题分析:G通过加聚反应生成高分子化合物甲,由甲的结构可知,G为![]() ,试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,苯甲醛与乙醛,在稀OH-、加热条件下生成D,由反应信息②可知,D为
,试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,苯甲醛与乙醛,在稀OH-、加热条件下生成D,由反应信息②可知,D为![]() ,D催化氧化生成E,故E为
,D催化氧化生成E,故E为![]() ,E与氢氧化钠反应生成F,故F为
,E与氢氧化钠反应生成F,故F为![]() ,F与C反应生成G与NaCl,根据G的结构可知,C为
,F与C反应生成G与NaCl,根据G的结构可知,C为![]() ,A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,氧原子数目为
,A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,氧原子数目为![]() =1,碳元素的质量分数为29.81%,碳原子的数目为
=1,碳元素的质量分数为29.81%,碳原子的数目为![]() =2,碳原子与氧原子的相对原子质量为12+16=28,故A含有1个Cl原子,A分子H原子数目为
=2,碳原子与氧原子的相对原子质量为12+16=28,故A含有1个Cl原子,A分子H原子数目为![]() =5,故A的分子式为C2H5OCl,A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2:2:1,则A的结构简式为ClCH2CH2OH,由反应信息①可知,B为ClCH2CH2OCH2CH2Cl,B在氢氧化钠醇溶液、加热条件下,发生部分消去反应生成
=5,故A的分子式为C2H5OCl,A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2:2:1,则A的结构简式为ClCH2CH2OH,由反应信息①可知,B为ClCH2CH2OCH2CH2Cl,B在氢氧化钠醇溶液、加热条件下,发生部分消去反应生成![]() 。
。
(1)由上述分析可知,A为ClCH2CH2OH,故答案为:ClCH2CH2OH;
(2)试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,B→C是ClCH2CH2OCH2CH2Cl氢氧化钠醇溶液、加热条件下,发生部分消去反应生成![]() ,故答案为:乙醛,消去反应;
,故答案为:乙醛,消去反应;
(3)①根据信息①,A→B的方程式为2ClCH2CH2OH ![]() ClCH2CH2OCH2CH2Cl+H2O,故答案为:2ClCH2CH2OH
ClCH2CH2OCH2CH2Cl+H2O,故答案为:2ClCH2CH2OH ![]() ClCH2CH2OCH2CH2Cl+H2O;
ClCH2CH2OCH2CH2Cl+H2O;
②D→E是![]() 催化氧化生成
催化氧化生成![]() ,反应方程式为:2
,反应方程式为:2![]() +O2
+O2![]() 2
2![]() +H2O,故答案为:2
+H2O,故答案为:2![]() +O2
+O2![]() 2
2![]() +H2O;
+H2O;
③C与F的反应是![]() 与
与![]() 生成
生成![]() 与NaCl,反应方程式为:
与NaCl,反应方程式为:![]() +
+![]()
![]()
![]() +NaCl,故答案为:
+NaCl,故答案为:![]() +
+![]()
![]()
![]() +NaCl;
+NaCl;
(4)![]() 的一种同分异构体,水解产物有两种,说明该异构体含有酯基,一种水解产物能使溴水褪色,故该异构体中含有C=C双键,另一种水解产物在滴加饱和溴水后,有白色沉淀生成,该产物中含有酚羟基,故该异构体含有羧酸酚酯,故该物质的结构简式为
的一种同分异构体,水解产物有两种,说明该异构体含有酯基,一种水解产物能使溴水褪色,故该异构体中含有C=C双键,另一种水解产物在滴加饱和溴水后,有白色沉淀生成,该产物中含有酚羟基,故该异构体含有羧酸酚酯,故该物质的结构简式为![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】锰的化合物种类较多,也大多具有广泛的用途。
I. MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性。某化学兴趣小组通过实验探究MnO2的性质。
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是____________。
A.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把MnO2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2SO3溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeSO4溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸。现象记录如下:

①从以上实验中,我们可以得出的结论是_________________________________。
②写出C试管中发生反应的离子方程式:_________________________________。
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机。MnFe2O4的制备工艺流程如下图:

已知Fe3+、Mn2+沉淀的pH为上表所示。
①步骤一中投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比理论上应为_____________________。
②步骤二中需控制pH的范围是 ___________ 。
③步骤三中是否洗涤干净的判断方法是 _______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质的说法正确的是
A.液态HCl不导电,所以HCl不是电解质
B.NH3溶于水形成的溶液能导电,所以NH3是电解质
C.稀硫酸能导电,所以稀硫酸是电解质
D.BaSO4在水溶液中难导电,但熔融状态下能导电,所以BaSO4是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.糖类化合物都具有相同的官能团
B.糖类是提供能量最高的营养物质
C.蛋白质的水解产物都含有羧基和氨基
D.酯类在碱性条件下的水解反应称为皂化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y元素最高正价与最低负价的绝对值之差是4;Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
A. KCl B. Na2S C. Na2O D. K2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
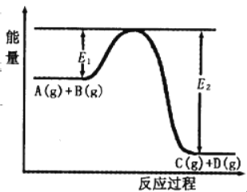
(1)该反应是______反应(填“吸热”“放热”);
(2)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1______,E2______(填“增大”“减小”、“不变”)。
(3)反应体系中加入催化剂对反应热是否有影响?______,(填“是”或“否”)原因是_______________。
(4)该反应的反应热△H=__________kJ/mol。(用E1和E2表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学方程式为___ ___。利用反应6NO2+8NH3=7N2+12H2O也可以处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______L。
(2)已知:2SO2(g)+O2(g) ![]() 2SO3(g) △H= -196.6kJ/mol
2SO3(g) △H= -196.6kJ/mol
2NO(g)+O2(g) ![]() 2NO2(g) △H= -113.0kJ/mol
2NO2(g) △H= -113.0kJ/mol
则反应NO2(g)+SO2(g) =SO3(g)+NO(g)的△H=______kJ/mol。
(3)如下图所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的SO2和O2使三容器压强相等,一定条件下发生2SO2(g)+O2(g) ![]() 2SO3(g)的反应。问:
2SO3(g)的反应。问:
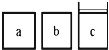
①起始a、c两容器的反应速率大小关系为Va_____Vc;(填“>”“<”或“=”下同)
②反应一段时间后a、c中速率大小关系为Va_____Vc;
③如起始在a、c两容器中通入等量的He,则此时三容器起始压强为Pa_____Pb_____Pc;起始反应速率关系为Va_____Vb_____Vc。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
据此回答以下问题:
(1)①该反应的化学平衡常数表达式为K=________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越________。
(2)某温度下,若把1 mol N2与3 mol H2置于体积为1L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为1/3,则该温度下反应的K的计算式=________(用分数表示)。能说明该反应达到化学平衡状态的是________(填字母)。
a.容器内的密度保持不变
b.容器内压强保持不变
c.v正(N2)=2v逆(NH3)
d.混合气体中c(NH3)不变
(3)对于合成氨反应而言,下列有关图像一定正确的是(选填序号)________。

(4)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a________b(填“>”、“=”或“<”,下同),Q1________Q2,Q1________92.4。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com