
【题目】氮元素的化合物种类繁多,性质也各不相同.
(1)图1为一定温度下1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图.已知E1=147.5kJmol﹣1 , E2=376.2kJmol﹣1(E1、E2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E1(填“增大”、“减小”或“不变”).该反应的热化学方程式为 . 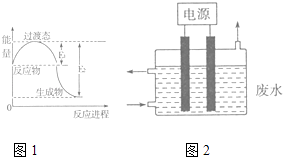
(2)硝基苯甲酸乙酯在OH﹣存在的条件下发生水解反应:
O2NC6H4COOC2H5+OH﹣O2NC6H4COOO﹣+C2H5OH
两种反应物的初始浓度均为0.050molL﹣1 , 某温度下测得O2NC6H4COOC2H5的转化率α随时间变化的数据如下表所示:
t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
α/% | 0 | 33 | 42 | 49 | 59 | 73 | 74 | 75 | 75 |
回答下列问题:①该反应在330s~530s的平均反应速率为(只列算式,不做运算)
②为提高O2NC6H4COOC2H5的转化率,可以采取的措施有 . (写1条即可)
(3)2015年8月12日天津港爆炸中有一定量的氰化物泄露,可用如图2所示装置除去含CN﹣、Cl﹣废水中的CN﹣ , 控制溶液pH为9~10,阳极产生的ClO﹣将CN﹣氧化为两种无污染的气体,该反应的离子方程式为 , 其中两个电极的材料分别为石墨和铁,则石墨作极,其电极反应式为 .
【答案】
(1)减小;NO2(g)+CO(g)=NO(g)+CO2(g)△H=﹣228.7KJ/mol
(2)![]() ;增加OH﹣的浓度、移去产物
;增加OH﹣的浓度、移去产物
(3)2CN﹣+5ClO﹣+H2O═N2↑+2CO2↑+5Cl﹣+2OH﹣;阳;Cl﹣+2OH﹣﹣2e﹣═ClO﹣+H2O
【解析】解:(1.)若在反应体系中加入催化剂,能降低反应的活化能,反应速率增大,则E1减小,图象分析可知一定温度下1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中,反应的焓变△H=E1﹣E2=147.5KJ/mol﹣376.2kJ/mol﹣=﹣228.7KJ/mol,该反应的热化学方程式为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=﹣228.7KJ/mol,所以答案是:减小,NO2(g)+CO(g)=NO(g)+CO2(g)△H=﹣228.7KJ/mol;
(2.)①该反应在330s~530s的平均反应速率= ![]() ,
,
所以答案是; ![]() ;
;
②为提高O2NC6H4COOC2H5的平衡转化率,可使平衡向正向移动,可增加OH﹣的浓度、移去产物,所以答案是:增加OH﹣的浓度、移去产物;
(3.)阳极产生的ClO﹣将CN﹣氧化为两种无污染的气体,两种气体为二氧化碳和氮气,该反应在碱性条件下进行,所以应该有氢氧根离子生成,反应方程式为2CN﹣+5ClO﹣+H2O═N2↑+2CO2↑+5Cl﹣+2OH﹣ , 该电解质溶液呈碱性,电解时,用不活泼金属或导电非金属作负极,可以用较不活泼金属作正极,石墨做阳极,阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,所以阳极反应式为Cl﹣+2OH﹣﹣2e﹣═ClO﹣+H2O,所以答案是:2CN﹣+5ClO﹣+H2O═N2↑+2CO2↑+5Cl﹣+2OH﹣ , 阳,Cl﹣+2OH﹣﹣2e﹣═ClO﹣+H2O.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)).


科目:高中化学 来源: 题型:
【题目】现有氧化铁和氧化铜的混合物m g,向其中加入100mL 3mol·L-1硝酸,恰好完全溶解,若m g该混合物在过量氢气流中加热充分反应,则冷却后剩余固体的质量为 ( )
A. (m-1.6)g B. (m-2.4)g C. (m-3.2)g D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的书写及对应表述均正确的是
A.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g 时,放出19.12 kJ 热量。则Fe(s)+S(s)![]() FeS(s) △H=95.6 kJmol1
FeS(s) △H=95.6 kJmol1
B.足量稀醋酸与 0.1 molL1NaOH 溶液反应:H+(aq)+OH(aq) ![]() H2O(l) △H=57.3 kJmol1
H2O(l) △H=57.3 kJmol1
C.已知,1 mol H2完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为:2H2O(l)![]() 2H2(g)+O2(g) △H=285.5kJmol1
2H2(g)+O2(g) △H=285.5kJmol1
D.已知 2C(s)+O2(g)![]() 2CO(g) △H= 221kJmol1,则可知 C 的燃烧热△H=110.5 kJmol1
2CO(g) △H= 221kJmol1,则可知 C 的燃烧热△H=110.5 kJmol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,下列物质占体积最大的是( )。
A. 64g H2O B. 6.02×1023个氮分子 C. 44.8L HCl D. 6g氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国已发射“嫦娥I号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO4)分解提供。高氯酸铵分解有可能排入大气的物质是 ( )
A.H2OB.SO2C.CO2D.CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)按如图电解氯化钠的稀溶液可制得漂白液,写出该电解池中发生反应的总反应方程式:; 
(2)将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从植物中分离出的化合物 zeylastral 的结构简式如图所示,下列说法不正确的是( ) 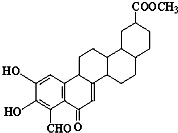
A.该化合物可以发生水解反应
B.该化合物能发生银镜反应
C.该化合物能使酸性KMnO4溶液褪色
D.该化合物共含有四种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池和电解池都能实现能量的置换.回答下列问题:
(1)可将化学能转化为电能是池;
(2)下列反应能设计成原电池的是:
①2FeCl3+Fe═3FeCl2 . Com]
②AlCl3+3NH3H2O═Al(OH)3↓+3NH4Cl
③NaOH+HCl═NaC1+H2O
(3)用FeCl3溶液腐蚀印刷电路铜板的离子方程式为:
(4)如图装置当闭合电键时,电表显示有电流通过.则Pt极的电极反应式:当甲中产生0.1mol气体时,乙中析出铜的质量应为g. 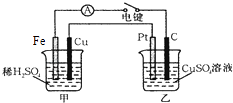
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示3套实验装置,分别回答下列问题.
(1)装置1为铁的吸氧腐蚀实验.向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 .
(2)装置2中的石墨是极(填“正”或“负”)
(3)装置3中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红.
①电源的M端为极;铁电极的电极反应
②停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64g,甲烧杯中产生的气体标准状况下体积为 mL.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com