
【题目】分类是学习和研究化学物质及其变化的一种常用的科学方法,下列分类不正确的是( )
A.纯碱、烧碱均属碱类
B.甲烷、乙醇、葡萄糖均属于有机物
C.盐酸、硫酸、硝酸均属酸类
D.糖类、油脂、蛋白质均属于营养物质
科目:高中化学 来源: 题型:
【题目】通过海水晒盐可以得到粗盐,粗盐除含 NaCl 外,还含有少量 MgCl2、CaCl2、Na2SO4、KCl 以及泥沙等物质。以下是甲、乙同学在实验室中粗盐提纯的操作流程。

提供的试剂:Na2CO3 溶液、K2CO3溶液、NaOH 溶液、BaCl2 溶液、75%乙醇。
(1)欲除去溶液 I 中的 MgCl2、CaCl2、Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为____。
A. 过量的 NaOH 溶液、Na2CO3 溶液、BaCl2 溶液
B. 过量的 NaOH 溶液、K2CO3、BaCl2 溶液
C. 过量的 NaOH 溶液、BaCl2 溶液、Na2CO3 溶液
D. 过量的 NaOH 溶液、BaCl2 溶液、K2CO3 溶液
(2)如何检验所加 BaCl2 溶液已过量____。
(3)在滤液中加盐酸的作用是_____。盐酸____(填“是”或“否”)可以过量。
(4)在洗涤的时候,可以使用的最佳洗涤剂是_____。
(5)乙同学欲使用提纯得到的精盐配制 100mL 1mol/L 的 NaCl 溶液,需要称量 NaCl____g,需使用的玻 璃仪器除了烧杯、玻璃棒和胶头滴管还有_____。
(6)甲同学观察乙同学的操作,认为他配制的溶液浓度偏低,乙同学可能做的错误操作有____。
A. 定容时,仰视读数
B. 洗涤容量瓶后没有进行干燥
C. 未洗涤烧杯和玻璃棒 2 次~3 次
D. 在定容时加水超过刻度线,再用胶头滴管吸出多余部分
E. 加水至刻度线后,摇匀过程中,发现液面低于刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1(T1=25℃)和T2时,水溶液中水的离子积曲线如图所示:下列判断错误的是( )

A. T2>25℃ B. x=1.0×10﹣7
C. KW(a)=KW(d) D. b点溶液呈碱性,c点溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛在航天、潜海和医疗方面应用广泛。工业上用钛铁矿(主要成分为钛酸亚铁FeTiO3,含FeO、Fe2O3、SiO2)为原料制TiO2,再由TiO2制得金属Ti

资料:TiO2+会发生水解
(1)步骤②、③、④中,均需用到的操作是_______。(填操作名称)
(2)检验滤液2中是否含Fe3+的方法是:_______。
(3)步骤1中FeTiO3溶于过量硫酸的化学方程式___________。

(4)请结合化学用语解释步骤④中加热水的原因___________。
(5)电解法获得Ti是通过图装置,以熔融CaCl2做电解质
①a为电源的_____(填“正”或“负”)
②在制备钛的过程中石墨电极附近的气泡中除了O2、CO、CO2外还可能有的气体是______________,用化学用语解释原因________________。
(6)测定废液中Fe2+浓度已确认铁元素的回收率:取25.00ml废液于锥形瓶中,用硫酸酸化的xmol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积如图所示:
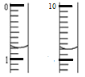
(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O).废液中c(Fe2+)=_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂空气电池如图甲,电池的工作原理如图乙。下列有关说法正确的是

A. 放电时,纸张中的纤维素作为锂电池的负极
B. 充电时,若阳极放出1molO2,则有4mol e-回到电源正极
C. 开关K闭合给锂电池充电,X对应充电电极上的反应为Li++e-=Li
D. 放电时,Li+由正极经过有机电解质溶液移向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温常压下,氯气的摩尔质量等于71 g
B. 1 mol H2SO4中含有2 mol氢元素
C. 某物质的摩尔质量就是该物质的相对分子质量或相对原子质量
D. 2 g氦气所含的原子数目约为0.5×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:H2(g)+I2(g)![]() 2HI(g)ΔH<0,现有三个相同的1L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1molH2和1molI2(g),在Ⅱ中充入2molHI(g),在Ⅲ中充入2molH2和2molI2(g),700℃条件下开始反应。达到平衡时,下列说法正确的是
2HI(g)ΔH<0,现有三个相同的1L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1molH2和1molI2(g),在Ⅱ中充入2molHI(g),在Ⅲ中充入2molH2和2molI2(g),700℃条件下开始反应。达到平衡时,下列说法正确的是
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ中反应的平衡常数大于容器Ⅲ中反应的平衡常数
C. 容器Ⅱ中的气体颜色比容器Ⅰ中的气体颜色深
D. 容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空
(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子数之比为___;氧原子数之比为____;相同条件下的体积之比为____。
(2)标准状况下,1.7gNH3与标准状况下___LH2S含有相同数目的氢原子。
(3)某气体氧化物的化学式为RO2,标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为____,R的相对原子质量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是
A. 等物质的量的NaN3和Na2O2中所含阴离子数均为NA
B. 14.2g C10H22中含有共价键总数为3.1NA
C. 标准状况下,将3.36L Cl2通入1L 0.2mol/L FeBr2溶液中,被氧化的Br-数目为0.3NA
D. 标准状况下,11 g由3H和16O组成的超重水中,中子数和电子数之和为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com