
【题目】有A、B、C、D四种易溶于水的白色固体,分别由Na+、Ba2+、Cu2+、Ag+、Cl-、SO42-、CO32-、NO3-中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A__________;D__________。
(2)写出下列反应的离子方程式:
①B+D→:________________;③C+HCl→气体:_______________。
(3)在作实验反思时,有同学提出:如果溶液中同时存在CO32- 和Cl-,CO32- 会对Cl- 的检验产生干扰。为了确定该溶液中是否存在Cl-,该小组同学进行了如下探究实验:
 _________________________________
_________________________________
【答案】AgNO3 BaCl2 SO42-+Ba2+=BaSO4↓ CO32-+2H+=H2O+CO2↑
实验操作 | 实验目的 | 反应的离子方程式 |
CO32- |
| |
AgNO3溶液 | Cl- | Cl-+Ag+=AgCl↓ |
【解析】
有A、B、C、D四种易溶于水的白色固体,分别由Na+、Ba2+、Cu2+、Ag+、Cl-、SO42-、CO32-、NO3-中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色,说明B中含有铜离子,铜离子不能与CO32-共存,故B为铜盐且不为碳酸铜;②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,白色沉淀为氯化银,Ag+与Cl-、SO42-、CO32-不能共存,所以A盐为AgNO3;C盐溶液中有较多气泡产生,产生的气体为二氧化碳,说明C盐中含有CO32-,而CO32-与Ba2+、Cu2+、Ag+均可发生反应,故C盐为Na2CO3,而D盐溶液无明显现象,D盐中含有Ba2+,由于Ba2+与SO42-不能共存,故D盐为BaCl2,则B盐为CuSO4。
(1)根据上述实验事实A为AgNO3、D为BaCl2。
(2)根据以上分析可知B+D的离子反应方程式为SO42-+Ba2+=BaSO4↓;C+HCl→气体的离子方程式为CO32-+2H+=H2O+CO2↑。
(3)要排除碳酸根离子对氯离子的干扰,需要首先除去碳酸根离子,可以加入过量的HNO3溶液除去碳酸根离子。检验氯离子一般用硝酸银溶液,即向第一步实验后的溶液中滴加硝酸银溶液来检验氯离子,离子方程式为Cl-+Ag+=AgCl↓。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】物质的下列性质能肯定该物质为离子化合物的是( )
A.水溶液能导电的化合物
B.由金属元素和非金属元素组成的化合物
C.在熔化状态下能导电的化合物
D.熔点高的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂为了节能减排,将烟道气中SO2和含Ca(OH)2、NaOH的废碱液作用,经过一系列化学变化,最终得到石膏和过二硫酸钠(Na2S2O8)。设计简要流程如图:
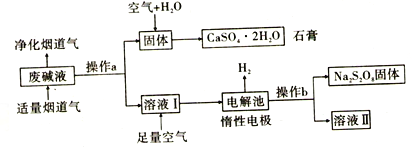
(1)操作a的名称是____________________。废碱液经操作a得到的固体为___________(填化学式)。
(2)向溶液I中通入足量的空气发生反应的化学方程式为_____________________________。
(3)已知用惰性电极电解SO42-可生成S2O82-,其过程如下图所示,S2O82-中S的化合价为__________,阳极生成Na2S2O8的电极反应式为____________________________;在整个流程中可以循环利用的物质是H2O和_________________ (填化学式)。
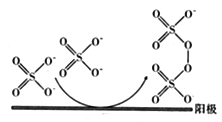
(4)若制取1mol Na2S2O8且阳极有11.2L的氧气产生(标准状况)。则电解生成的H2在标准状况下的体积为______________L。
(5)烟道气中的SO2可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1 (H2SO3)=1.8×10-2,Ka2 (H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学。下列是中学化学中一些常见的实验装置,按要求回答下列问题:
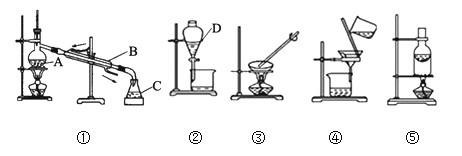
(1)写出仪器名称:D__________。
(2)装置①中的错误是_______________________________。
(3)分离下列混合物的实验操作中,用到实验装置②的是______,用到装置⑤的是________(填字母代号)。
A.水和泥沙的混合物 B.水和酒精的混合物
C.水和四氯化碳的混合物 D.淀粉胶体和氯化钠溶液
E.固体氯化钠和碘单质 F.碳酸钙和碳酸钠粉末
(4)粗盐提纯所需装置为_________和___________,操作过程中均要用到玻璃棒,玻璃棒的作用分别是________________、_________________。
(5)装置②可用于CCl4萃取碘水中的碘,如何检验萃取后的碘水中还存在碘单质_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】80年代,科学研制得一种新分子,它具有空心的类似足球状的结构,分子式为C60 . 下列说法正确的是( )
A.C60是一种新型的化合物
B.C60含有离子键
C.C60和金刚石互为同位素
D.C60中的化学键只有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法中,不利于实现让海南“天更蓝,山更绿,水更清”目标的是( )
A.污水未经处理直接排入大海B.推广使用清洁能源
C.植树进林,提高森林覆盖率D.推广使用无磷洗涤剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在反应 KMnO4+ HCl= MnCl2+ KCl+ Cl2↑+ H2O中,MnCl2为易溶于水的强电解质,回答下列问题:
①氧化剂是___________,还原剂是__________;
②配平上述方程式并用双线桥法标明电子转移的方向和数目:______________;
③写出上述反应的离子方程式:_________________________________________;
④若生成71gCl2,被氧化的HCl是_________________g。
(2)单质铁与稀HNO3可发生多种反应,当8/3n(Fe)<n(HNO3)≤4n(Fe)时,反应方程式可用下列通式表示:aFe+bHNO3(稀)=cNO十dFe(NO3)2+eFe(NO3)3十fH2O。
①假设a=16,且b、c、d、e、f均取正整数时,共有_______组系数配比。
②若a、b、c、d、e、f符合上述系数的配比关系,则b与C的关系为:b=____c。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图分别表示生物体内生物大分子的部分结构模式图,据图回答:
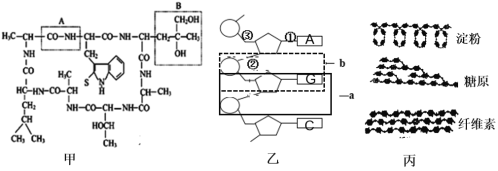
(1)从甲、乙、丙可以看出,生物大分子都是以_________为基本骨架。甲图中A结构名称为__________。
(2)乙图所示化合物的基本组成单位是_____________,各单体间通过_______(用序号表示)相连。如果该链表示RNA的一部分结构,则图示未表示出来的含氮碱基名称是___________ ;如果该链表示DNA的一部分结构,则图示未表示出来的含氮碱基名称是___________ ,图b表示的核苷酸名称为__________________________。
(3)丙图所示三种物质中,在功能上与另外两种截然不同的物质是_________,它可以参与植物细胞中__________(填某细胞结构)的构成 。丙图中三种物质的单体都是__________,该物质为还原糖,常用__________检测;而甲一般用____________检测,两种试剂使用方法的区别是前者需要__________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com