
【题目】下列各有机物的数目与分子式C4H7ClO2且能与NaHCO3溶液反应生成CO2的有机物的数目(不考虑立体异构)相同的是
A.分子式为C5H10的烯烃B.甲苯的一氯代物
C.相对分子质量为74的一元醇D.立方烷(![]() )的二硝基取代物
)的二硝基取代物
【答案】A
【解析】
分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有ClCH2-CH2-CH2COOH,CH3-CHCl-CH2COOH,CH3-CH2-CHClCOOH,CH2Cl-CH(CH3)COOH,CH3-CCl(CH3)COOH共5种。
A.因为戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、![]() 、
、 ,对于CH3-CH2-CH2-CH2-CH3,相应烯烃有:CH2=CH-CH2-CH2-CH3、CH3-CH=CH-CH2-CH3,其中CH3-CH=CH-CH2-CH3有2种顺反异构,即有3种结构;对于
,对于CH3-CH2-CH2-CH2-CH3,相应烯烃有:CH2=CH-CH2-CH2-CH3、CH3-CH=CH-CH2-CH3,其中CH3-CH=CH-CH2-CH3有2种顺反异构,即有3种结构;对于![]() ,相应烯烃有:CH2=C(CH3)CH2CH3;CH3C(CH3)=CHCH3;CH3CH(CH3)CH=CH2,都不存在顺反异构,即有3种结构;对于
,相应烯烃有:CH2=C(CH3)CH2CH3;CH3C(CH3)=CHCH3;CH3CH(CH3)CH=CH2,都不存在顺反异构,即有3种结构;对于 ,没有相应烯烃,所以分子式为C5H10的烯烃共有3+3=6种(包括顺反异构),本题不考虑立体异构,所以为5种,故A正确;
,没有相应烯烃,所以分子式为C5H10的烯烃共有3+3=6种(包括顺反异构),本题不考虑立体异构,所以为5种,故A正确;
B.甲苯的一氯代物共有4种,如下:①取代甲基上的氢原子;②取代与甲基相邻的苯环上的氢原子;③取代与甲基相间的苯环上的氢原子;④取代与甲基相对位置的苯环上的氢原子,故B错误;
C.根据相对分子质量为74的一元醇:74-16=58,58÷14=4……2,所以化学式为:C4H10O,因为丁基有4种,所以分子式为C4H10O的醇有4种,故C错误;
D.立方烷的二硝基取代物有3种,分别是取代到棱上的两个、面对角线上的两个、体对角线上的两个,故D错误。
故选A。


科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中一定能大量共存的是
A.无色透明溶液:K+、H+、MnO4-、SO32-
B.0.1mol/LCuSO4溶液:Mg2+、Al3+、NO3-、C1-
C.![]() =1×1013mol/L溶液:K+、Fe2+、SCN-、NO3-
=1×1013mol/L溶液:K+、Fe2+、SCN-、NO3-
D.能与金属铝反应产生H2的溶液:Na+、NH4+、CO32-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铁水滑石(镁、铁的碱式碳酸盐)是具有层状结构的无机功能材料,可由Mg(NO3)2·6H2O、Fe(NO3)3·9H2O及CO(NH2)2等按一定比例在温度高于90℃时反应制得。
(1)其他条件不变时,n[CO(NH2)2]/n(Fe3+)对镁铁水滑石产率和溶液pH的变化关系如图所示:
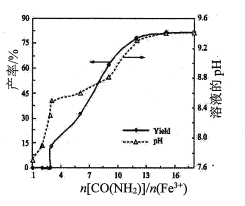
①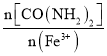 <3,反应液中产生少量气体,测氨仪未检出NH3,说明逸出的气体主要是____________(填化学式)。
<3,反应液中产生少量气体,测氨仪未检出NH3,说明逸出的气体主要是____________(填化学式)。
②n[CO(NH2)2]/n(Fe3+)>12,溶液的pH处于稳定状态,这是因为_________________
(2)镁铁水滑石表示为:[FexMgy(OH)z](CO3)w·pH2O(摩尔质量为660g·mol-1),可通过下列实验和文献数据确定其化学式,步骤如下:
I.取镁铁水滑石3.300g加入足量稀硫酸充分反应,收集到气体112mL(标准状况)。
II.文献查得镁铁水滑石热分解TG-DSC图:303~473K,失去层间水(结晶水)失重为10.9%;473~773K时,CO32-和OH-分解为CO2和H2O;773K以上产物为MgO、Fe2O3。
Ⅲ.称取0.4000g热分解残渣(773K以上)置于碘量瓶中,加入稍过量盐酸使其完全溶解,加入适量水和稍过量的KI溶液,在暗处放置片刻,用0.1000mol·L-1Na2S2O3标准溶液滴定到溶液呈淡黄色,加入3mL淀粉溶液,继续滴定到溶液蓝色消失。(2Na2S2O3+I2=2NaI+Na2S4O6),消耗Na2S2O3溶液20.00mL。通过计算确定镁铁水滑石的化学式______________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJmol-1
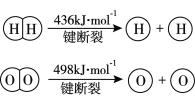
下列说法不正确的是
A. 该反应可作为氢氧燃料电池的反应原理
B. 破坏1mol H-O键需要的能量是463.4 kJ
C. H2O(g)=H2(g) +1/2O2(g) ΔH = +241.8 kJmol-1
D. H2(g)中的H-H键比H2O(g)中的H-O键牢固
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组尝试在钢制钥匙上镀铜。
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。
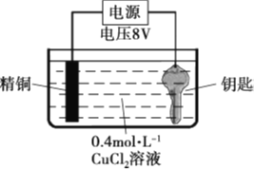
实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是_______。
(2)实验II中钥匙应与电源的_______极连接。
(3)钥匙表面产生的气体是_______。
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是________。
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是________。(已知CuOH是一种难溶于水的黄色固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是2SO3(g)![]() 2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
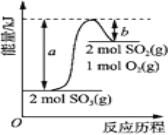
A. 该化学反应过程中既有能量的吸收又有能量的释放
B. 2SO3(g)![]() 2SO2(g)+O2(g) △H=-(a-b) kJ/mol
2SO2(g)+O2(g) △H=-(a-b) kJ/mol
C. 1 mol SO2的能量比1 mol SO3的能量高
D. 若某容器内有2 mol SO3充分反应,吸收(a-b) kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】补铁剂常用于防治缺铁性贫血,其有效成分一般为硫酸亚铁、琥珀酸亚铁、富马酸亚铁和乳酸亚铁等。回答下列问题:
(1)能表示能量最低的亚铁离子的电子排布式是_________(填标号)。
a.[Ar]3d54s2 b.[Ar]3d54s1 c.[Ar]3d64s2 d.[Ar]3d6
(2)琥珀酸即丁二酸(HOOCCH2CH2COOH),在琥珀酸分子中电负性最大的原子是_____,碳原子的杂化方式是______;琥珀酸亚铁中存在配位键,在该配位键中配位原子是____,中心原子是____。
(3)富马酸和马来酸互为顺反异构体,其电离常数如下表:
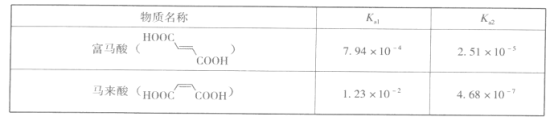
请从氢键的角度解释富马酸两级电离常数差别较小,而马来酸两级电离常数差别较大的原因:____。
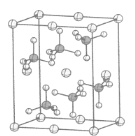
(4)β-硫酸亚铁的晶胞结构如图所示,其晶胞参数为a= 870 pm、b=680 pm、c=479 pm,α=β=γ=90°,Fe2+占据晶胞顶点、棱心、面心和体心。在该晶胞中,硫酸根离子在空间上有____种空间取向,晶胞体内硫酸根离子的个数是____,铁原子周围最近的氧原子的个数为____;设阿伏加德罗常数的值为NA,则该晶体的密度是____ g·cm-3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是( )
A.SO2与Ba(NO3)2反应生成BaSO3
B.NH3在纯O2中燃烧生成NO2
C.过量CO2与氨水反应生成NH4HCO3
D.高温条件下Fe与水蒸气反应生成Fe(OH)3和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为充分利用资源,变废为宝,实验室里利用废铁屑制取硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]。某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。

已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。请回答下列问题:
(1)步骤②中,H2C2O4稍过量的主要原因是________。
(2)为了提高步骤③得到的FeC2O4·2H2O的纯度,宜用________(填“热水”“冷水”或“无水乙醇”)洗涤,检验洗涤是否干净的操作是________。
(3)实现步骤④必须用到的两种仪器是________(供选仪器:a. 烧杯;b. 坩埚;c. 蒸馏烧瓶;d. 高温炉;e. 表面皿;f. 锥形瓶)。
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________。
(5)硫酸亚铁铵是重要的工业原料,其溶解性如表所示:
10 | 20 | 30 | 40 | 50 | 60 | |
(NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
FeSO4·7H2O | 40.0 | 48.0 | 60.0 | 73.3 | — | — |
(NH4)2Fe(SO4)2·6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(注意:高于73.3℃,FeSO4·7H2O发生分解)
以铁屑(有油污)、硫酸、硫酸铵为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,______,冷却,过滤,用蒸馏水洗涤铁屑至中性,将铁屑置于锥形瓶中,_____至铁屑完全溶解,_____,冷却结晶,用无水乙醇洗涤2~3次,低温干燥。[实验中必须使用的试剂:铁屑、1.0 mol·L-1的Na2CO3溶液、3.0 mol·L-1的H2SO4溶液,饱和(NH4)2SO4溶液]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com