
【题目】已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)请根据上述信息判断下列反应不能发生的是 (填编号).
A.CH3COOH+NaCN═CH3COONa+HCN
B.CO2+H2O+2NaClO═Na2CO3+2HClO
C.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
D.HCN+Na2CO3→NaCN+CO2+H2O
(2)已知常温时Ksp(AgCl)=1.8×10﹣10mol2L﹣2 , 向50mL 0.18molL﹣1的AgNO3溶液中加入相同体积0.22molL﹣1的盐酸,则c(Ag+)= .
【答案】
(1)BD
(2)9.0×10﹣8mol/L
【解析】解:(1)六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,
A.CH3COOH酸性大于HCN,反应CH3COOH+NaCN═CH3COONa+HCN能发生,故A正确;
B.酸性H2CO3>HClO>HCO3﹣ , 应生成NaHCO3 , 反应CO2+H2O+2NaClO═Na2CO3+2HClO不能发生,故B错误;
C.酸性C6H5OH>HCO3﹣ , 反应Na2CO3+C6H5OH→NaHCO3+C6H5ONa能发生,故C正确;
D.酸性H2CO3>C6H5OH>HCO3﹣ , 反应生成碳酸氢钠,正确反应为CO2+H2O+C6H5ONa→NaHCO3+C6H5OH反,故D错误,
故答案为:BD;(2)向50mL 0.018molL﹣1的AgNO3溶液中加入相同体积0.020molL﹣1的盐酸,盐酸过量,反应后的c(Cl﹣)= ![]() =0.002mol/L,
=0.002mol/L,
则:c(Ag+)= ![]() mol/L=9×10﹣8mol/L,
mol/L=9×10﹣8mol/L,
故答案为:9.0×10﹣8 mol/L.
(1)六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,根据强酸生成弱酸的特点判断反应能否进行;(2)先判断过量,然后计算出混合液中氯离子的浓度,最后根据氯化银溶度积常数进行计算c(Ag+).


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图1转化关系(部分生成物和反应条件已略去). 
(1)若A为金属钠,A与水反应的离子方程式为 .
(2)若A为过氧化钠,A与水反应的化学方程式为 .
(3)A不论是Na还是Na2O2 , 依据转化关系判断物质D是 ,
(4)向30ml某浓度的B溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有如图2所示两种情况(不计CO2的溶解),则曲线B表明M中的溶质为;原NaOH溶液的物质的量浓度为;由曲线A、B可知,两次实验通入的CO2的体积比为 .
(5)Na2CO3和NaHCO3浓度均为0.1mol/L的混合溶液中,离子浓度由小到大的顺序是请你设计一实验证明Na2CO3溶液碱性比NaHCO3溶液的碱性强: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生使用托盘天平称食盐时,错误的将食盐放在右托盘,而把砝码放在左托盘,称得食盐的质量为15.5g(1g以下只能使用游码)。.如果按正确的方法,食盐的质量应为
A. 15.5g B. 15.0g C. 14.5g D. 14.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应①Fe(s)+CO2(g)FeO(s)+CO(g)△H1=akJmol﹣1 , 平衡常数为K;反应②CO(g)+ ![]() O2(g)CO2(g)△H2=bkJmol﹣1 . 测得在不同温度下,K值如表:
O2(g)CO2(g)△H2=bkJmol﹣1 . 测得在不同温度下,K值如表:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)若500℃时进行反应①,CO2起始浓度为2mol/L,CO的平衡浓度为 .
(2)反应①中的a0(填“大于”、“小于”或“等于”).
(3)700℃时反应①达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有(填序号).
A.缩小反应器体积
B.通入CO2
C.升高温度到 900℃
D.使用合适的催化剂
(4)如图图象符合反应①的是(填序号)(图中φ是混合物中CO的含量;T为温度).
(5)反应③2Fe(s)+O2(g)═2FeO(s)△H3= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是( )
A.酯化反应的反应物之一肯定是乙醇
B.酯化反应一般需要吸水
C.酯化反应中反应物不能全部转化为生成物
D.酯化反应一般需要催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知金属活动相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题: 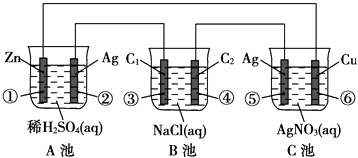
(1)各装置名称是:A池 , B池 .
(2)写出电极上发生的反应:① , ③ , ⑤ .
(3)当电路上有2mol电子流过时,①极上质量变化g,⑥极上质量变化g.
(4)反应进行一段时间后,A,B,C三池中电解质溶液浓度不变的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com