
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
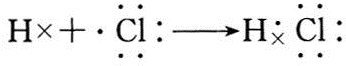 ;B与G形成离子化合物(填“离子”或“共价”),用电子式表示它的形成过程
;B与G形成离子化合物(填“离子”或“共价”),用电子式表示它的形成过程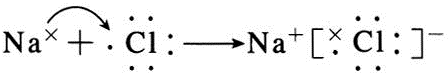 .
. 分析 由元素在周期表中的位置可知,A为H,B为Na,C为Al,D为C,E为N,F为P,G为F,H为Cl,I为Ne.
(1)稀有气体原子最外层为稳定结构,化学性质最不活泼;F元素非金属性最强,只有负化合价,单质氧化性最强;上述元素中,Na的金属性最强,则其单质还原性最强;
(2)金属性越强,最高价氧化物对应水化物的酸性最强;最高价氧化物的水化物中酸性最强的是高氯酸;氢氧化铝能与酸、碱反应生成盐与水,属于两性氢氧化物;
(3)A与H形成的化合物为HCl,属于共价化合物;B与G形成的化合物为NaF,属于离子化合物.
解答 解:由元素在周期表中的位置可知,A为H,B为Na,C为Al,D为C,E为N,F为P,G为F,H为Cl,I为Ne,
(1)以上元素中,只有Ne的最外层电子为8,为稳定结构,则化学性质不活泼,F的非金属性最强,氟元素没有正化合价,只有负化合价,F2的氧化性最强,上述元素中,Na的金属性最强,则其单质还原性最强,
故答案为:Ne;F;F2;Na;
(2)上述元素中,Na的金属性最强,则最高价氧化物的水化物NaOH的碱性最强,最高价氧化物的水化物中酸性最强的是HClO4,上述元素中的最高价氧化物的水化物中只有Al(OH)3为两性,
故答案为:NaOH;HClO4;Al(OH)3;
(3)A与H形成的化合物为HCl,属于共价化合物,用电子式表示形成过程为: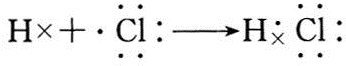 ;B与G形成的化合物为NaF,属于离子化合物,用电子式表示形成过程为
;B与G形成的化合物为NaF,属于离子化合物,用电子式表示形成过程为 ,
,
故答案为:共价;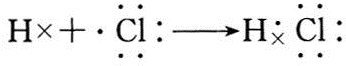 ;离子;
;离子; .
.
点评 本题考查元素周期律与元素周期律综合应用,侧重元素周期律与化学用语考查,注意用电子式表示化学键或物质的形成,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取3.23 g NaCl固体 | |
| B. | 用10 mL 量筒量取 7.50 mL 稀盐酸 | |
| C. | 分液以后 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 | |
| D. | 稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与盐酸反应的化学方程式为:FeS2+2HCl═FeCl2+S↓+H2S↑ | |
| B. | 在FeS2中,硫元素的化合价与辉铜矿(主要成分是Cu2S)中硫元素的化合价相同 | |
| C. | FeS2中的Fe元素位于第4周期第ⅧB族 | |
| D. | 若FeS2在空气中燃烧时生成Fe2O3和SO2,则1mol FeS2在反应中将失去6mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量醋酸钠晶体后,两溶液的pH均增大 | |
| B. | 将温度升高至50℃,两溶液的pH均不变 | |
| C. | 加水稀释至原体积的2倍后,两溶液的pH均减小 | |
| D. | 加入足量锌粉充分反应后,两溶液产生氢气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑥ | B. | ②⑦ | C. | ①③④ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核内质子数为131 | B. | 核内中子数为131 | C. | 原子序数为53 | D. | 质量数为53 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用燃煤脱硫技术,防止SO2污染 | |
| B. | 采用绿色化学生产工艺,提高原子利用率 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采力度,增加化石燃料的供应量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某烷烃CnH2n+2的一个分子中,含有共价键的数目是3n+1 | |
| B. | 用HNO3酸化的AgNO3溶液检验CCl4中是否含有氯元素 | |
| C. | 红热的铜丝可以和乙醇发生置换反应产生氢气 | |
| D. | 石油化工得到的产品均为液体,煤化工得到的产品有液体也有固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com