
(1)水下发射导弹时常采用一种火箭燃料肼(N2H4)。已知在101kPa时,32.0g液态的N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式为_______________________。
(2)我国科学家在1973年就已经将上述反应设计成燃料电池,该燃料电池的电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时:
①正极的电极反应式为_______________________。
②负极的电极反应式为_______________________。
(3)用N2H4做火箭燃料常采用N2O4做氧化剂,反应得到的产物对环境无害,则反应的化学方程式为:______________________。
科目:高中化学 来源:2016届浙江省高三上学期月考(三)化学试卷(解析版) 题型:选择题
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,再向所得浊液中逐渐加入 1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。下列说法不正确的是( )
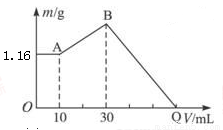
A.A点沉淀是Mg(OH)2
B.AB段发生的离子反应是AlO2-+H++H2O =Al(OH)3↓
C.原混合物中NaOH的质量是5.20g
D.Q点时耗用的HCl体积120ml
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:选择题
在下列各说法中,正确的是
A.ΔH > 0表示放热反应,ΔH < 0表示吸热反应
B.1 mol H2与0.5 mol O2反应的焓变就是H2的燃烧热
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀的焓变叫做中和热
D.热化学方程式中的化学计量数表示物质的量,可以是分数
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高一上学期期中测试化学试卷(解析版) 题型:选择题
下列溶液中Cl-浓度最大的是
A.200mL 2 mol·L—1 MgCl2溶液
B.1000mL 2.5 mol·L—1 NaCl溶液
C.300mL 5 mol·L—1 KCl溶液
D.250mL 1 mol·L—1 AlCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期期中联考化学试卷(解析版) 题型:选择题
研究发现CuSO4和FeS2在一定条件下可发生如下反应: 14CuSO4+5FeS2+12H2O =7Cu2S +5FeSO4 +12H2SO4;下列说法正确的是
A.FeS2中的硫元素全部被氧化
B.5 mol FeS2发生反应,有10 mol电子转移
C.产物中SO42-有一部分是氧化产物
D.FeS2只用作还原剂
查看答案和解析>>
科目:高中化学 来源:2016届湖南省澧县、桃源、益阳三校高三上学期联考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.氢气是一种环保、可再生的能源
B.电解熔融AlCl3可制金属铝
C.可溶性铁盐或铝盐常用于水的净化
D.二氧化硅可用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三上学期统练(三)化学试卷(解析版) 题型:填空题
(1)已知:25℃时,Ksp[Mg(OH)2]=4×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
①25℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为 。
②25℃时,向该Mg(OH)2饱和溶液中加入适量稀盐酸达平衡后该溶液中c(OH-) , c(Mg2+)(填“增大”“减小”或“不变”) 。
(2)向50 mL 0.018 mol/L的AgNO3溶液中加入50 mL 0.020 mol/L的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液的体积变化,请计算:
①充分反应后,溶液中c(Ag+)= mol/L。
②充分反应后,溶液的pH= 。
(3)如图,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-物质的量浓度的对数,回答下列问题。
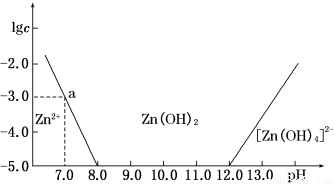
①往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为__________。
②从图中数据计算可得Zn(OH)2的溶度积Ksp=________。
③某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是___________________。
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第四次考试化学试卷(解析版) 题型:选择题
下列日常生活中的现象与氧化还原反应无关的是( )
A.铜铸塑像上出现铜绿[Cu2(OH)2CO3]
B.用石膏点豆腐
C.不良商贩用硫黄熏蒸法制作“白豆芽”
D.自来水厂用氯气对水进行消毒
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:填空题
(Ⅰ)室温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
实验 编号 | HA的物质的量 浓度(mol/L) | NaOH的物质的 量浓度(mol/L) | 混合后 溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸? 。
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=________mol/L。
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B===H++HB- HB- H++B2-
H++B2-
回答下列问题:
(5)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
(III)已知:25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
(6)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释)_____________。万一误服了少量BaCO3,应尽快用大量0.5 mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为_____mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com