
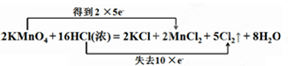
 (2分)
(2分) ;
;

科目:高中化学 来源:不详 题型:单选题
| A.0.448 L | B.0.672 L | C.0.896 L | D.0.224 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用该方法检验管道泄漏处会产生白烟 |
| B.管道泄漏处会闻到刺激性气味 |
| C.该反应生成1mol氮气时,转移3mol电子 |
| D.可以用浸有稀碱液的布包裹在管道泄漏处,暂时防止氯气的危害 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2作还原剂 |
| B.碱性条件下,NaIO3的氧化性强于Na2H3IO6 |
| C.每生成1 mol Na2H3IO6,转移2 mol电子 |
| D.氧化产物与还原产物的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 +3
+3 +aH+=2Cr3++3Y+4H2O下列说法不正确的是
+aH+=2Cr3++3Y+4H2O下列说法不正确的是A.Y是 |
| B.a=8 |
C. 被氧化成 被氧化成 |
D.生成1 mol 时转移的电子数是3×6.02×1023 时转移的电子数是3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2 mol/L | B.1 mol/L | C.0.4 mol/L | D.0.2 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com