
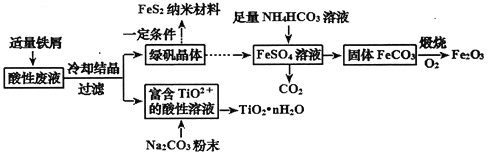
【题目】利用钛矿的酸性废液(含TiO2+、Fe2+、Fe3+、SO42-等),可回收获得FeS2纳米材料、Fe2O3和TiO2·nH2O等产品,流程如下:
(1)TiO2+中钛元素的化合价为________价。TiO2+只能存在于强酸性溶液中,因为TiO2+易水解生成TiO2·nH2O,写出水解的离子方程式_________________________________。
(2)向富含TiO2+的酸性溶液中加入Na2CO3粉末能得到固体TiO2·nH2O。请用化学反应原理解释__________________________________。
(3)NH4HCO3溶液与FeSO4溶液反应的离子方程式为_______________________,该反应需控制温度在308K以下,其目的是_____________________________。
(4)已知298K时,Ksp[Fe(OH)2]=8.0×10-16,若在生成的FeCO3达到沉淀溶解平衡时,测得溶液的pH为8.5,c(Fe2+)=1.0×10-5mol·L-1,则所得的FeCO3中________Fe(OH)2(填“有”或“没有”)。
(5)FeS2纳米材料可用于制造高容量锂电池,已知电解质为熔融的K2S,电池放电时的总反应为:4Li+FeS2=Fe+2Li2S,则正极的电极反应式是_______________。
【答案】+4 TiO2++(n+1)H2O![]() TiO2nH2O+2H+ 碳酸钠消耗H+,c(H+)减小,使TiO2+水解平衡向生成TiO2nH2O方向移动 Fe2++2HCO3- =FeCO3↓+CO2↑+H2O 防止NH4HCO3受热分解和减少Fe2+的水解 没有 FeS2+4e-﹦Fe+2S2-
TiO2nH2O+2H+ 碳酸钠消耗H+,c(H+)减小,使TiO2+水解平衡向生成TiO2nH2O方向移动 Fe2++2HCO3- =FeCO3↓+CO2↑+H2O 防止NH4HCO3受热分解和减少Fe2+的水解 没有 FeS2+4e-﹦Fe+2S2-
【解析】
酸性废液(含TiO2+、Fe2+、Fe3+、SO42-等)中加入适量铁屑,发生反应2Fe3++Fe==3Fe2+,冷却结晶后,Fe2+转化为绿矾晶体;绿矾晶体溶于水得FeSO4溶液,往溶液中加入足量的NH4HCO3溶液,发生反应生成CO2气体和FeCO3沉淀等;FeCO3固体在O2中煅烧,可生成Fe2O3和CO2;富含TiO2+的酸性溶液中加入Na2CO3粉末,能得到固体TiO2·nH2O,同时应生成CO2。
(1)TiO2+中,O元素显-2价,则钛元素的化合价为+4价。TiO2+只能存在于强酸性溶液中,因为TiO2+易水解生成TiO2·nH2O,表明TiO2+结合H2O中的O,生成H+,则水解的离子方程式为TiO2++(n+1)H2O![]() TiO2nH2O+2H+。答案为:+4;TiO2++(n+1)H2O
TiO2nH2O+2H+。答案为:+4;TiO2++(n+1)H2O![]() TiO2nH2O+2H+;
TiO2nH2O+2H+;
(2)向富含TiO2+的酸性溶液中加入Na2CO3粉末能得到固体TiO2·nH2O,同时应生成CO2气体。用化学反应原理解释为碳酸钠消耗H+,c(H+)减小,使TiO2+水解平衡向生成TiO2nH2O方向移动。答案为:碳酸钠消耗H+,c(H+)减小,使TiO2+水解平衡向生成TiO2nH2O方向移动;
(3)NH4HCO3溶液与FeSO4溶液反应,生成CO2气体和FeCO3沉淀等,离子方程式为Fe2++2HCO3- =FeCO3↓+CO2↑+H2O,该反应需控制温度在308K以下,主要从NH4HCO3的热稳定性和Fe2+的水解两方面考虑,其目的是防止NH4HCO3受热分解和减少Fe2+的水解。答案为:Fe2++2HCO3- =FeCO3↓+CO2↑+H2O;防止NH4HCO3受热分解和减少Fe2+的水解;
(4)溶液的pH为8.5,则pOH=5.5,c(OH-)=1.0×10-5.5mol·L-1,c(Fe2+)=1.0×10-5mol·L-1,则c(Fe2+) c2(OH-)=1.0×10-5×(1.0×10-5.5)2=1.0×10-16<8.0×10-16,故所得的FeCO3中没有Fe(OH)2。答案为:没有;
(5)电解质为熔融的K2S,由电池放电时的总反应:4Li+FeS2=Fe+2Li2S,可确定正极反应为FeS2得电子生成Fe和S2-,电极反应式是FeS2+4e-﹦Fe+2S2-。答案为:FeS2+4e-﹦Fe+2S2-。


科目:高中化学 来源: 题型:
【题目】某兴趣小组设计了如下实验测定海带中碘元素的含量,依次经过以下四个步骤,下列图示装置和原理能达到实验目的的是
A.灼烧海带
B.将海带灰溶解后分离出不溶性杂质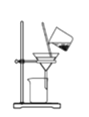
C.制备Cl2,并将I-氧化为I2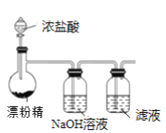
D.以淀粉为指示剂,用Na2SO3标准溶液滴定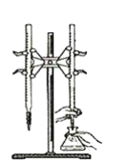
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是无色具有水果香味的液体,沸点为77.2℃,实验室某次制取它用冰醋酸14.3mL、95%乙醇23mL,还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液,主要装置如图所示:

实验步骤:
①先向A中的蒸馏烧瓶中注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用。这时分液漏斗里冰醋酸和乙醇的物质的量之比约为5∶7。
②加热油浴保温约135 ℃~145℃
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加入速率使蒸出酯的速率与进料速率大体相等,直到加料完成。
④保持油浴温度一段时间,至不再有液体馏出后,停止加热。
⑤取下B中的锥形瓶,将一定量饱和Na2CO3溶液分批少量多次地加到馏出液里,边加边振荡,至无气泡产生为止。
⑥将⑤的液体混合物分液,弃去水层。
⑦将饱和CaCl2溶液(适量)加入到分液漏斗中,振荡一段时间后静置,放出水层(废液)。
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品。
试回答:
(1)实验中浓硫酸的主要作用是_________________________。
(2)用过量乙醇的主要目的是____________________________。
(3)用饱和Na2CO3溶液洗涤粗酯的目的是_______________________。
(4)用饱和CaCl2溶液洗涤粗酯的目的是_______________________。
(5)在步骤⑧所得的粗酯里还含有的杂质是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到。
![]() +H2SO4
+H2SO4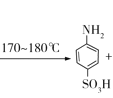 H2O
H2O
已知:苯胺是一种无色油状液体,微溶于水,易溶于乙醇,熔点6.1℃,沸点184.4℃。对氨基苯磺酸是一种白色晶体,微溶于冷水,可溶于沸水,易溶于碱性溶液,不溶于乙醇。实验室可用苯胺、浓硫酸为原料,利用如图所示实验装置合成对氨基苯磺酸。
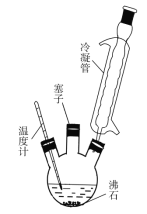
实验步骤如下:
步骤1:在250 mL三颈烧瓶中加入10 mL苯胺及几粒沸石,将三颈烧瓶放在冰水中冷却,小心地加入18 mL浓硫酸。
步骤2:将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5小时。
步骤3:将反应产物冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出。将烧瓶内残留的产物冲洗到烧杯中,抽滤,洗涤,得到对氨基苯磺酸粗产品。
步骤4:将粗产品用沸水溶解,冷却结晶,抽滤,收集产品,晾干可得纯净的对氨基苯磺酸。
(1)装置中冷凝管的作用是__________。
(2)步骤2油浴加热的优点有____________________。
(3)步骤3中洗涤沉淀的操作是______________。
(4)步骤3和4均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先__________,然后__________,以防倒吸。
(5)若制得的晶体颗粒较小,分析可能的原因______(写出两点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学习小组的同学设计了如下图所示装置验证SO2的某些性质。下列说法正确的是

A. Ⅰ中浓硫酸表现强氧化性
B. Ⅱ中紫色石蕊溶液先变红后褪色
C. Ⅲ中硫化氢溶液用于验证SO2的氧化性
D. Ⅲ中两个棉球均褪色,加热后均又恢复原来颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中对应关系正确的是
A | CH3CH3+Cl2 | 均为取代反应 |
B | 由油脂得到甘油 | 均发生了水解反应 |
C | Cl2+2Br=2Cl+Br2 | 均为单质被还原的置换反应 |
D | 2Na2O2+2H2O+4NaOH+O2↑ | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应来说,以下化学反应速率的表示中反应速率最快的是( )
A.v(NH3)=0.6mol·L-1·s-1B.v(O2)=0.4mol·L-1·s-1
C.v(N2)=0.2mol·L-1·s-1D.v(H2O)=1.2mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是

A. 复分解反应、复分解反应、化合反应、置换反应
B. 中和反应、置换反应、复分解反应、置换反应
C. 复分解反应、复分解反应、置换反应、置换反应
D. 分解反应、复分解反应、置换反应、置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
A. 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
B. 2.3g钠在空气中燃烧生成多种氧化物是转移电子数为0.1NA
C. 1.8g D2O中含有的质子数为1.0NA
D. 235g核素![]() 发生裂变反应
发生裂变反应![]() +
+ ![]()
![]()
![]() Sr+
Sr+![]() Xe+10
Xe+10![]() n,净产生的中子(
n,净产生的中子(![]() n)数为10NA
n)数为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com