
【题目】过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
(1)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体转化为二氧化碳和水,达到无害化.有关甲醛、苯、二氧化碳及水说法正确的是_____。
①苯与B3N3H6的总电子数相等;
②甲醛、苯分子中碳原子均采用sp3杂化;
③苯、二氧化碳、水和甲醛都是非极性分子;
④水的沸点比甲醛高得多,是因为水分子间能存在氢键,甲醛分子间不存在氢键。
(2)2007年诺贝尔物理学奖为法国科学家阿尔贝费尔和德国科学家彼得格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就.某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca,Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。
①用A,B,O表示这类特殊晶体的化学式:_______ 。
②Cr、Mn的核外特征电子排布式分别为:Cr:[Ar]3d54s1、Mn:[Ar]3d54s2,则它们第一电离能由小到大的排列顺序是:_______用“<”排列)。
(3)CO2的空间构型为______;固体CO2与SiO2熔沸点差异很大的原因是________
(4)冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图2)类似,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有__个水分子;冰晶胞与金刚石晶胞微粒排列方式相同的原因是_______ 。

【答案】①④ ABO3 Cr<Mn 直线型分子 CO2是分子间作用力形成的分子晶体,SiO2是共价键形成的空间网状原子晶体 8 水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子可与相邻的4个水分子形成氢键,且为正四面体结构
【解析】
(1)①苯的电子总数为6×6+6=42,B3N3H6的的电子总数为3×5+3×7+6=42;
②甲醛、苯分子中碳原子均形成3个σ键,二氧化碳中碳原子均形成2个σ键,均没有孤电子对;
③分子中正负电荷中心重合的为非极性分子,正负电荷中心不重合的为极性分子;
④水分子之间形成氢键,沸点较高;
(2)①利用均摊法计算晶胞中所含各原子的个数,再根据原子数之比确定化学式;
②Mn的4s上有2个电子,4s处于全充满,较稳定;Cr的4s上只有1个电子。
(3)根据价层电子对互斥理论确定其空间构型,根据不同类型晶体的性质差异比较熔沸点;
(4)利用均摊法确定每个冰晶胞含有的水分子个数,根据氧原子和碳原子的杂化方式以及氢键的特点,分析冰晶胞与金刚石晶胞微粒排列方式相同的原因。
(1)①苯的电子总数为6×6+6=42,B3N3H6的的电子总数为3×5+3×7+6=42,所以苯与B3N3H6的总电子数相等,故①正确;
②甲醛、苯分子中碳原子均形成3个σ键,二氧化碳中碳原子形成2个σ键,均没有孤电子对,甲醛、苯分子中碳原子采用sp2杂化,二氧化碳分子中C原子采取sp杂化,故②错误;
③苯、二氧化碳分子的空间结构对称是非极性分子,甲醛分子的空间结构不对称属于极性分子,水分子中的氧原子有孤对电子,水分子为V形,水分子是极性分子,故③错误;
③水的沸点比甲醛高得多,是因为水分子间能形成氢键,故④正确。
故答案为:①④。
(2)①由图1可知,晶胞中A位于顶点,晶胞中含有A为8×1/8=1个,B位于晶胞的体心,含有1个,O位于面心,晶胞中含有O的个数为6×1/2=3,则化学式为ABO3,
故答案为:ABO3。
②Mn的4s上有2个电子,4s处于全充满,较稳定;Cr的4s上只有1个电子,Cr失去4s上的1个电子形成较稳定的价电子结构(3d5);第一电离能由小到大的排列顺序为:Cr<Mn,故答案为:Cr<Mn。
(3)二氧化碳分子中碳原子价层电子对数是2,且不含孤电子对,所以其空间构型是直线形。CO2是分子晶体,分子间是范德华力,SiO2是空间网状结构的原子晶体,原子之间是共价键,共价键键能远大于范德华力,所以固体CO2的熔沸点比SiO2熔沸点要小得多,
故答案为:直线型分子;CO2是分子间作用力形成的分子晶体,SiO2是共价键形成的空间网状原子晶体。
(4)每个冰晶胞平均占有分子个数=4+8×1/8+6×1/2=8,H2O的氧原子形成2个σ键、含2对孤电子对,金刚石中每个碳原子含有4个σ键且没有孤电子对,所以水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子中一个氧原子可以和另外2个水分子形成氢键,2个氢原子可以和另外2个水分子形成氢键,所以每个水分子可与相邻的4个水分子形成氢键,导致冰晶胞与金刚石晶胞微粒排列方式相似,
故答案为:8;水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子可与相邻的4个水分子形成氢键,且为正四面体结构。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】如图是中国在南极建设的第四个科学考察站——泰山站。为了延长科学考察站基础设施使用寿命,钢铁设备表面镶嵌一些金属块(M)。下列说法正确的是

A. 金属块M可能是铜,发生氧化反应
B. 这种保护方法叫牺牲阳极的阴极保护法
C. 科考考察站里的设备在潮湿空气中主要发生化学腐蚀
D. 若采用外加电流的阴极保护法,设备与电源正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列正确的叙述有( )
①CO2、NO2、P2O5均为酸性氧化物,MgO、Fe2O3、Na2O2均为碱性氧化物
②Ca(HCO3)2 、FeS、FeCl3均可由化合反应制得
③按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、盐酸、苛性钾、次氯酸、氨气
④需要通电才可进行的有:电离、电解、电泳
A.1个B.2个C.3个D.4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则A极的电极反应式为____________________
B极的Fe发生__________ 腐蚀(填“析氢”或“吸氧”)
(2)若开始时开关K与b连接,下列说法正确的是________(填序号)
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
且此时装置内总反应的离子方程式为________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用工业大理石(含有少量SiO2、Al2O3、Fe2O3等杂质)制取CaCl2·6H2O,设计了如下流程:
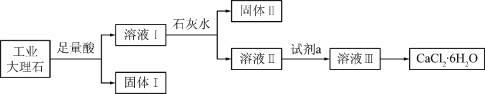
下列说法不正确的是
A. 固体I中含有SiO2,固体II中含有Fe(OH)3
B. 使用石灰水时,要控制pH,防止固体II中Al(OH)3转化为AlO2-
C. 试剂a选用盐酸,从溶液III得到CaCl2·6H2O产品的过程中,须控制条件防止其分解
D. 若改变实验方案,在溶液I中直接加氨水至沉淀完全,滤去沉淀,其溶液经蒸发浓缩、冷却结晶也可得到纯净CaCl2·6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示。下列说法一定正确的是( )
A. 最高正化合价:Z>X
B. X、Y、Z的单质中,Z的熔点最高
C. 若X为非金属元素,则离子半径:Xn->Ym->Zm-
D. 若X为金属元素,则X、Y、Z的最高价氧化物对应水化物中,Y的碱性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制氨气的化学方程式为_________________________。
(2)0.1 mol/LNH4Cl溶液中离子浓度由大到小的顺序为____________________。
(3)已知0.5mol的液态甲醇(CH3OH)在空气中完全燃烧生成CO2气体和液态水时放出350kJ的热量,则表示甲醇燃烧热的热化学方程式为______________________。
(4)已知①C(s)+O2(g)= CO2(g) ΔH1=-393 kJ/mol
②2CO(g)+O2(g)= 2CO2(g) ΔH2=-566 kJ/mol
③TiO2(s)+2Cl2(g)= TiCl4(s)+O2(g) ΔH3=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s)= TiCl4(s)+2CO(g)的 ΔH =__________________。
(5)在25℃下,向浓度均为0.1 mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀_____(填化学式)(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20)。
(6)常温下,0.lmol/LNaHCO3溶液的pH大于8,则溶液中c(H2CO3)______c(CO32-)(填“>”、“=”或“<”)。
(7)在25℃下,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应完成后溶液中c(NH4+)=c(Cl-),则溶液显_________性(填“酸”“碱”或“中”),a _________0.01 mol/L(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是
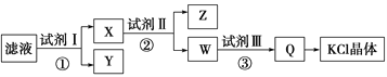
A. 起始滤液的pH=7
B. 试剂Ⅰ为Ba(NO3)2溶液
C. 步骤②中加入试剂Ⅱ的目的是除去Ba2+
D. 图示的步骤中必须要经过2次过滤操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为1L的密闭容器中,0.3molX和0.2molY进行反应:2X(g)+Y(s) ![]() Z(g),经10s达到平衡,生成0.1molZ。下列说法正确的是( )
Z(g),经10s达到平衡,生成0.1molZ。下列说法正确的是( )
A. 若增加Y的物质的量,则V正大于V逆平衡正向移动
B. 以Y浓度变化表示的反应速率为0.01mol·L-1·s-1
C. 该反应的平衡常数为10
D. 若降低温度,X的体积分数增大,则该反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com