
【题目】(1)实验室制氨气的化学方程式为_________________________。
(2)0.1 mol/LNH4Cl溶液中离子浓度由大到小的顺序为____________________。
(3)已知0.5mol的液态甲醇(CH3OH)在空气中完全燃烧生成CO2气体和液态水时放出350kJ的热量,则表示甲醇燃烧热的热化学方程式为______________________。
(4)已知①C(s)+O2(g)= CO2(g) ΔH1=-393 kJ/mol
②2CO(g)+O2(g)= 2CO2(g) ΔH2=-566 kJ/mol
③TiO2(s)+2Cl2(g)= TiCl4(s)+O2(g) ΔH3=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s)= TiCl4(s)+2CO(g)的 ΔH =__________________。
(5)在25℃下,向浓度均为0.1 mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀_____(填化学式)(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20)。
(6)常温下,0.lmol/LNaHCO3溶液的pH大于8,则溶液中c(H2CO3)______c(CO32-)(填“>”、“=”或“<”)。
(7)在25℃下,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应完成后溶液中c(NH4+)=c(Cl-),则溶液显_________性(填“酸”“碱”或“中”),a _________0.01 mol/L(填“>”、“=”或“<”)。
【答案】2NH4C1+Ca(OH)2![]() 2NH3↑+CaC12+2H2O c(Cl-)>c(NH4+)>c(H+)>c(OH-) CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-700kJ/mol -79 kJ/mol Cu(OH)2 > 中 >
2NH3↑+CaC12+2H2O c(Cl-)>c(NH4+)>c(H+)>c(OH-) CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-700kJ/mol -79 kJ/mol Cu(OH)2 > 中 >
【解析】
(1)在实验室中是用铵盐与碱共热制取氨气的,反应的化学方程式是:2NH4C1+Ca(OH)2![]() 2NH3↑+CaC12+2H2O;
2NH3↑+CaC12+2H2O;
(2) NH4Cl是强酸弱碱盐,在溶液中NH4+发生水解反应,消耗水电离产生的OH-,当最终达到平衡后,溶液中c(H+)>c(OH-),NH4+由于水解而消耗,所以c(Cl-)>c(NH4+),盐电离产生的离子浓度大于水电离产生的离子浓度,所以c(NH4+)>c(H+),因此最终溶液中离子浓度大小关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(3)燃烧热是1mol可燃物完全燃烧产生稳定的氧化物时放出的热量,由于0.5mol甲醇完全燃烧产生CO2气体和液体水放出热量是350kJ,所以甲醇燃烧热的化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) △H=-700kJ/mol;
(4) ③+2×①-②,整理可得TiO2(s)+2Cl2(g)+2C(s)= TiCl4(s)+2CO(g)ΔH =-79kJ/mol;
(5)由于难溶性的物质Mg(OH)2、Cu(OH)2的构型相同,所以向浓度均为0.1 mol/L的MgCl2和CuCl2混合溶液中加入氨水水,溶度积常数小的物质,首先形成沉淀。由于Ksp[Mg(OH)2]=1.8×10-11<KsP[Cu(OH)2]=2.2×10-20,所以先形成Cu(OH)2沉淀;
(6) NaHCO3是强碱弱酸盐,在溶液中HCO3-既存在电离作用,产生H+和CO32-,也存在水解作用,产生H2CO3和OH-,电离产生H+是溶液显酸性;水解产生OH-,使溶液显碱性,由于常温下,0.lmol/LNaHCO3溶液的pH大于8,说明HCO3-的水解作用大于电离作用,故溶液中c(H2CO3)>c(CO32-);
(7)对于该溶液来说,存在电荷守恒,c(H+)+ c(NH4+)=c(OH-)+c(Cl-),由于c(NH4+)=c(Cl-),所以c(H+)=c(OH-),溶液显中性;盐酸是强酸,完全电离,一水合氨为弱碱,只有部分电离,现在c(H+)=c(OH-),所以c(NH3H2O)> c(OH-)= c(H+)=c(HCl)=0.01mol/L,即c(NH3H2O)>0.01mol/L。


科目:高中化学 来源: 题型:
【题目】改变0.1 mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知:δ(X)=![]() ]。下列叙述错误的是
]。下列叙述错误的是

A. K1(H2A)=10-1.2
B. pH=2.7时,c(H2A)+c(HA-)+c(A2-)=0.1 mol·L-1
C. pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D. pH=4.2时,c(HA-)=c(A2-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作____剂。
(2)自然界Cr主要以+3价和+6价存在。Cr2O72-的Cr能引起细胞的突变,在酸性条件下可以用亚硫酸钠将其还原为+3价的铬,写出其离子方程式_____________________________________________ :
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是______________。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下:

①上述操作中有多次过滤,其中玻璃棒的作用__________ ,向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为____。
②对滤液Ⅱ先加H2O2再调pH,调pH的目的是____。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
(1)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体转化为二氧化碳和水,达到无害化.有关甲醛、苯、二氧化碳及水说法正确的是_____。
①苯与B3N3H6的总电子数相等;
②甲醛、苯分子中碳原子均采用sp3杂化;
③苯、二氧化碳、水和甲醛都是非极性分子;
④水的沸点比甲醛高得多,是因为水分子间能存在氢键,甲醛分子间不存在氢键。
(2)2007年诺贝尔物理学奖为法国科学家阿尔贝费尔和德国科学家彼得格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就.某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca,Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。
①用A,B,O表示这类特殊晶体的化学式:_______ 。
②Cr、Mn的核外特征电子排布式分别为:Cr:[Ar]3d54s1、Mn:[Ar]3d54s2,则它们第一电离能由小到大的排列顺序是:_______用“<”排列)。
(3)CO2的空间构型为______;固体CO2与SiO2熔沸点差异很大的原因是________
(4)冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图2)类似,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有__个水分子;冰晶胞与金刚石晶胞微粒排列方式相同的原因是_______ 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式________。
(2)根据等电子原理,写出CO分子的结构式______。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是______________;甲醛分子中碳原子轨道的杂化类型为________。
②甲醛分子的空间构型是________;1 mol甲醛分子中σ键的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)元素①~⑧中,除⑧外,原子半径最大的是___________(填元素符号),元素③、⑦所形成的氢化物的稳定性由强到弱的顺序为__________________(用相应氢化物的化学式作答)元素②的氢化物的电子式是____________。
(2)④⑤⑥三种元素的氢氧化物的碱性由强到弱的顺序是________(用相应氢氧化物的化学式作答),元素①~⑧中的最高价氧化物对应的水化物中酸性最强的酸是_______(填化学式)。
Ⅱ.实验室用密度为1.84g/cm3,溶质的质量分数为98%的硫酸,配制980mL物质的量浓度为0.1mol/L的硫酸。供选用的仪器有:①胶头滴管;②药匙;③烧杯;④量筒;⑤托盘天平。请回答下列问题:
(1)配制上述溶液量取浓硫酸时应选用__________量筒(选填序号)
①10mL ②50mL ③100mL;
(2)配制稀硫酸时,上述仪器中还缺少的仪器有____________________________(写仪器名称),不需要使用的有______________(选填序号);
(3)下列操作使所配溶液的物质的量浓度偏低的是___________。
A.用量筒量取的浓硫酸,慢慢地沿着玻璃棒注入盛有20mL蒸馏水的小烧杯,搅拌后,立即转移到容量瓶中,再按正确操作配制溶液。
B.往容量瓶转移溶液时,有少量液体溅出。
C.未洗涤稀释浓硫酸的小烧杯
D.定容时俯视刻度线。
E.容量瓶未干燥即用来配制溶液。
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )
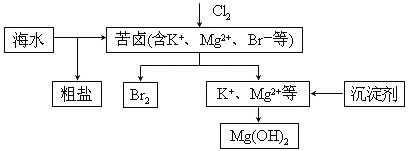
A. 向苦卤中通入Cl2是为了提取溴
B. 工业生产中常选用NaOH作为沉淀剂
C. 粗盐可采用除杂和重结晶等过程提纯
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用![]() 将其还原吸收
将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若某原子在处于能量最低状态时,外围电子排布为![]() ,则下列说法错误的是
,则下列说法错误的是
A. 该元素可能有+3价
B. 该元素位于第5周期副族
C. 该元素原子核外共有39个不同运动状态的电子
D. 该元素基态原子第N能层上还有5个空轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属保护的说法不正确的是 ( )
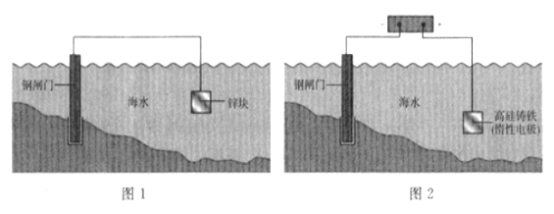
A. 图1是牺牲阳极阴极保护法,图2是外加电流阴极保护法
B. 钢闸门均为电子输入的一端
C. 锌和高硅铸铁的电板反应均为氧化反应
D. 两图所示原理均发生了反应:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com