
����Ŀ��һ�������£����Ϊ1L���ܱ������У�0.3molX��0.2molY���з�Ӧ��2X��g����Y��s�� ![]() Z��g������10s�ﵽƽ�⣬����0.1molZ������˵����ȷ���ǣ� ��
Z��g������10s�ﵽƽ�⣬����0.1molZ������˵����ȷ���ǣ� ��
A. ������Y�����ʵ�������V������V��ƽ�������ƶ�
B. ��YŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.01mol��L��1��s��1
C. �÷�Ӧ��ƽ�ⳣ��Ϊ10
D. �������¶ȣ�X���������������÷�Ӧ����H��0
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɽ���Ԫ���������Ӧ���о���Ŀǰ��ѧ�о���ǰ��֮һ���Իش��������⣺
��1������������������ܽ�������Ⱦ���ȩ�������к�����ת��Ϊ������̼��ˮ���ﵽ�������йؼ�ȩ������������̼��ˮ˵����ȷ����_____��
�ٱ���B3N3H6���ܵ�������ȣ�
�ڼ�ȩ����������̼ԭ�Ӿ�����sp3�ӻ���
�۱���������̼��ˮ�ͼ�ȩ���ǷǼ��Է��ӣ�
��ˮ�ķе�ȼ�ȩ�ߵö࣬����Ϊˮ���Ӽ��ܴ����������ȩ���Ӽ䲻���������
��2��2007��ŵ��������ѧ��Ϊ������ѧ�Ұ������Ѷ��͵¹���ѧ�ұ˵ø��ֱ������ͬ��ã��Ա��������ھŵ���ЧӦ��CMRЧӦ���о�����ijɾͣ�ij���������������ͼ1������Aԭ��Ϊ�����Ķ��㣬Aλ������Ca��Sr��Ba��Pb����Bλ��V��Cr��Mn��Feʱ�����ֻ��������CMRЧӦ��
����A��B��O��ʾ�������⾧��Ļ�ѧʽ��_______����
��Cr��Mn�ĺ������������Ų�ʽ�ֱ�Ϊ��Cr��[Ar]3d54s1��Mn��[Ar]3d54s2�������ǵ�һ��������С���������˳���ǣ�_______�á��������У���
��3��CO2�Ŀռ乹��Ϊ______������CO2��SiO2�۷е����ܴ��ԭ����________
��4����������ˮ���ӵĿռ����з�ʽ����ʯ�������侧���ṹ��ͼ2�����ƣ����п�������ʾԭ��λ��������Ķ�������ģ�ʵ������ʾԭ��λ���������ڣ����ƣ�ÿ��������ƽ��ռ��__��ˮ���ӣ�����������ʯ���������з�ʽ��ͬ��ԭ����_______����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijԭ���ڴ����������״̬ʱ����Χ�����Ų�Ϊ![]() ��������˵���������
��������˵���������
A. ��Ԫ�ؿ�����+3��
B. ��Ԫ��λ�ڵ�5���ڸ���
C. ��Ԫ��ԭ�Ӻ����39����ͬ�˶�״̬�ĵ���
D. ��Ԫ�ػ�̬ԭ�ӵ�N�ܲ��ϻ���5���չ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧͨ��ʵ���о�Na2O2��ˮ�ķ�Ӧ��
���� | ���� |
��ʢ������Na2O2���Թ��м�������ˮ���õ���Һa | ��Ӧ���ң�������ʹ������ľ����ȼ������ |
Ȼ������Һa�е������η�̪ | ��Һ�ȱ�죬����dz��Լ10������Һ��Ϊ��ɫ |
Ϊ��̽����Һ��Ϊ��ɫ��ԭ��ͬѧ���տ�ѧ�ij�����������ʵ�飺
����������裩
Na2O2��H2O��Ӧ�Ļ�ѧ����ʽ_____������Һa�еμӷ�̪��Ӧֻ���죬��ʵ���з��ַ�̪��������ɫ���ɴ�������µļ��裺
����A��O2��Ư���� ����B��NaOH��Ư���� ����C��O2��NaOH��ͬ������Ư����
��ʵ����۲죩
��2��������±���
ʵ���� | 1 | 2 | 3 |
ʵ��װ�� |
|
|
|
ʵ����� ���A������B����C���� | ����_____ | ����____ | ����__ |
ʵ������ | ��Һ����10���Ӿ��ޱ仯 | ||
ʵ����� | _____ | ||
���������ϣ�
��ͬѧ�������ϣ�H2O2��һ���ڼ��������²��ȶ�������Ư���Ե����ʡ�
����������裩
��ͬѧ��Ϊ��ɫ��ԭ���������Һa�д���H2O2��H2O2Ư���˷�̪��
��ʵ����۲죩
��3��ͨ��ʵ��֤ʵ��H2O2�Ĵ��ڣ�ȡ������Һa�������ɫ��ĩ____���ѧʽ�������ٲ�������ʹ������ľ����ȼ�����塣��ͬѧ��һ��ͨ��ʵ��֤ʵ����Һa�е����̪��H2O2���̪�����˻�ѧ��Ӧ��ʵ�鷽����ȡ������Һa���Թ��У�_____��
����������ۣ�
��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������![]() ��Һ�������жϲ���ȷ���� ( )
��Һ�������жϲ���ȷ���� ( )
A. ����������![]() ��Һ��ͬ
��Һ��ͬ
B. �����¶ȣ�![]() ����
����
C. ����![]() ��Һ��
��Һ��![]() ��С
��С
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£���100 mLNaOH��Һ�л���ͨ��һ������CO2���壬��ַ�Ӧ������������ҺM��PH��7����Ӧǰ����Һ������仯���Բ��ƣ�������ҺM����λ����μ�1 mol/L���ᣬ����������������������������ϵ��ͼ��ʾ��
��֪ͼ��B��λ�ù̶�����V(B)=300,����A C ���ڸ��Ե������ƶ���
��1��ԭ��Һ�����ʵ���Ũ��Ϊ_________mol/L��B��ʱ������������Һ�е����ʵ����ʵ���Ũ����___________mol/L(������Һ���ʱ�������ֱ�����)
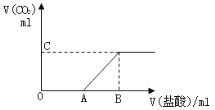
��2��V(A)��ȡֵ��ͬʱ����ҺM�е����ʵijɷ�Ҳ��ͬ������д�±���
V(A)��ȡֵ | V(A)��0 | 0��V(A)��150 | V(A)��150 | 150��V(A)��300 |
���ʵijɷ� | ��__________ | ��___________ | ��_________ | ��_____________ |
��V(A)��200ʱ��C����ֵΪ_____________��
��3��ȡV(A)��100ʱ��Ӧ����ҺM 30ml ��������1 mol/L�����ᰴ���ֿ��ܵķ�ʽ��ϣ��������������Vml,��V ��ȡֵ��Χ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ���������˵������ȷ���� ( )
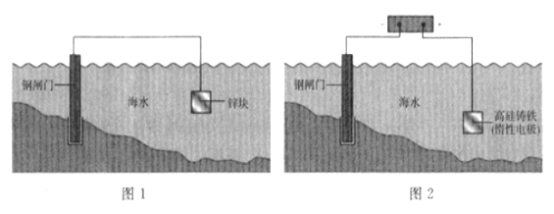
A. ͼ1����������������������ͼ2����ӵ�������������
B. ��բ�ž�Ϊ���������һ��
C. п�߹������ĵ�巴Ӧ��Ϊ������Ӧ
D. ��ͼ��ʾԭ���������˷�Ӧ:![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ����![]() �ζ�
�ζ�![]() ijһԪ��HX,�ζ�������pH�仯������ͼ��ʾ��
ijһԪ��HX,�ζ�������pH�仯������ͼ��ʾ��

����˵����ȷ����
A. HX��Һ�����Ե�ԭ����![]()
B. ��a��![]()
C. ��b��![]() ��
��![]() ǡ����ȫ��Ӧ
ǡ����ȫ��Ӧ
D. ��c��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������˵����ȷ���ǣ� ��
A.1 mol��������2NA����ԭ��B.14 g�����к�6.02��1023��������
C.���³�ѹ�£�32gO3���е�ԭ����Ϊ2NAD.18 gˮ�������ĵ�����ΪNA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com