
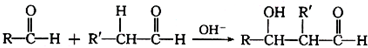
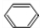
 ,苯与溴发生取代反应生成H为
,苯与溴发生取代反应生成H为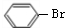 ,溴苯与氢气发生加成反应生成I,结合I的分子式可知,I为
,溴苯与氢气发生加成反应生成I,结合I的分子式可知,I为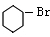 ,I发生卤代烃的水解反应生成J为
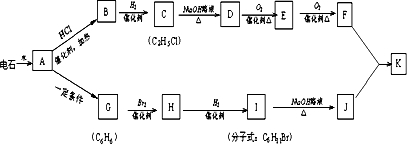
,I发生卤代烃的水解反应生成J为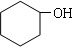 .乙炔与HCl发生加成反应生成B,B与氢气反应加成反应生成C,由C的分子式可知,B为CH2=CHCl,C为CH3CH2Cl,C发生卤代烃的水解反应生成D为CH3CH2OH,D发生氧化反应生成C为CH3CHO,C进一步发生氧化反应生成F为CH3COOH,F与J发生酯化反应生成K为
.乙炔与HCl发生加成反应生成B,B与氢气反应加成反应生成C,由C的分子式可知,B为CH2=CHCl,C为CH3CH2Cl,C发生卤代烃的水解反应生成D为CH3CH2OH,D发生氧化反应生成C为CH3CHO,C进一步发生氧化反应生成F为CH3COOH,F与J发生酯化反应生成K为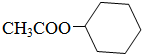 ,据此解答.
,据此解答. ,苯与溴发生取代反应生成H为
,苯与溴发生取代反应生成H为 ,溴苯与氢气发生加成反应生成I,结合I的分子式可知,I为
,溴苯与氢气发生加成反应生成I,结合I的分子式可知,I为 ,I发生卤代烃的水解反应生成J为
,I发生卤代烃的水解反应生成J为 .乙炔与HCl发生加成反应生成B,B与氢气反应加成反应生成C,由C的分子式可知,B为CH2=CHCl,C为CH3CH2Cl,C发生卤代烃的水解反应生成D为CH3CH2OH,D发生氧化反应生成C为CH3CHO,C进一步发生氧化反应生成F为CH3COOH,F与J发生酯化反应生成K为
.乙炔与HCl发生加成反应生成B,B与氢气反应加成反应生成C,由C的分子式可知,B为CH2=CHCl,C为CH3CH2Cl,C发生卤代烃的水解反应生成D为CH3CH2OH,D发生氧化反应生成C为CH3CHO,C进一步发生氧化反应生成F为CH3COOH,F与J发生酯化反应生成K为 ,
, +Br2
+Br2| Fe |
 +HBr,
+HBr, +Br2
+Br2| Fe |
 +HBr;
+HBr; | 醇 |
| △ |
| 醇 |
| △ |
| Cu |
| △ |
| Cu |
| △ |
| 催化剂 |
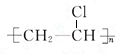 ,故答案为:n CH2=CHCl
,故答案为:n CH2=CHCl | 催化剂 |
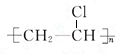 ;
; ,故答案为:
,故答案为: ;
;| OH- |
| OH- |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| ||
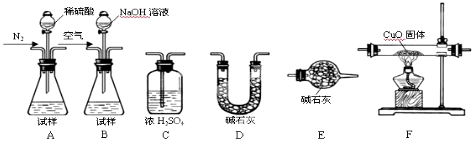
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中,当有1 mol铜被氧化时,被还原的硝酸为23 mol |
| B、某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015 mol |
| C、室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧.则a、b的关系为 a=4b+3c |
| D、物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比为1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3=2Na++CO32- |
| B、NaHSO4=Na++H++SO42- |
| C、NaHCO3=Na++HCO3- |
| D、KClO3=K++Cl-+3O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
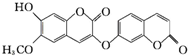 西瑞香素是具有较强的抗肿瘤活性药物,其结构简式如图所示.下列关于西瑞香素的结构和性质叙述正确的是( )
西瑞香素是具有较强的抗肿瘤活性药物,其结构简式如图所示.下列关于西瑞香素的结构和性质叙述正确的是( )| A、分子中所有原子可以处于同一平面 |
| B、该物质能发生加成、氧化、水解、消去等反应 |
| C、能与FeCl3溶液发生显色反应 |
| D、1 mol该有机物最多可与3 mol NaOH反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com