
【题目】为了确定某种矿质元素是否是植物的必需元素,应采用的方法是
A. 检测正常叶片中该矿质元素的含量
B. 分析根系对该矿质元素的吸收过程
C. 分析环境条件对该植物吸收矿质元素的影响
D. 观察在完全培养液中去掉该矿质元素前后植株的生长发育状况
科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2═P4O10 . 已知断裂下列化学键需要吸收的能量分别为:P﹣P akJmol﹣1、P﹣O b kJmol﹣1、P═O c kJmol﹣1、O═O d kJmol﹣1
根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )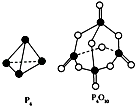
A.(6a+5d﹣4c﹣12b)kJmol﹣1
B.(4c+12b﹣6a﹣5d)kJmol﹣1
C.(4c+12b﹣4a﹣5d)kJmol﹣1
D.(4c+5d﹣4c﹣12b)kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有1mol HNO3的稀硝酸分别与不同质量的铁粉,所得氧化产物a、b与铁粉物质的量关系如图所示.下列有关判断正确的是( ) 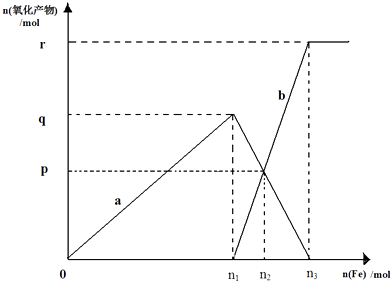
A.a是Fe(NO3)2
B.n1=0.375
C.p=0.20
D.n2=0.30
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式____________________________________。
(2)己知反应N2+3H2![]() 2NH3 △H=akJ/mol。试根据下表中所列键能数据估算a的数值为______。
2NH3 △H=akJ/mol。试根据下表中所列键能数据估算a的数值为______。
化学键 | H-H | N-H | N≡N |
键能kJ/mol | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
己知:C(s,石墨)+O2(g)=CO2(g) △Hl=-393. 5kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
2C2H2(g) +5O2(g) =4CO2(g) +2H2O(1) △H3=-2599kJ/mol
裉推盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应热化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲制备漂白剂亚氯酸钠(NaClO2)。甲同学通过查阅文献发现:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体的是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
实验I 乙同学利用下图所示装置制取NaClO2晶体

(l)装置B中生成了ClO2,反应的化学方程式为_________________________________。
(2)装置A和E的作用是_____________________。
(3)装置D中发生反应的化学方程式为_________________________________________。
(4)反应结束后,先将装置D反应后的溶液在55℃条件下减压蒸发结晶,然后进行的操作是_________________,再用38℃~60℃的温水洗涤,最后在低于60℃条件下干燥,得到NaClO2晶体。
实验Ⅱ 丙同学设计实验测定制得NaClO2样品的纯度
其实验步骤如下:
① 称取所得亚氯酸钠样品ag于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应后,配成100mL混合液。
② 取25.00 mL待测液于锥形瓶中,用bmol/LNa2S2O3标准液滴定,消耗标准液体积的平均值为VmL(已知:I2+2S2O32-=2I-+S4O62-)。
(5)步骤① 反应的离子方程式为__________________________________________。
(6)步骤② 滴定中使用的指示剂是____________________。
(7)样品中NaClO2的质最分数为_________________(用含a、b、V的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com