
【题目】白磷与氧可发生如下反应:P4+5O2═P4O10 . 已知断裂下列化学键需要吸收的能量分别为:P﹣P akJmol﹣1、P﹣O b kJmol﹣1、P═O c kJmol﹣1、O═O d kJmol﹣1
根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )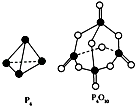
A.(6a+5d﹣4c﹣12b)kJmol﹣1
B.(4c+12b﹣6a﹣5d)kJmol﹣1
C.(4c+12b﹣4a﹣5d)kJmol﹣1
D.(4c+5d﹣4c﹣12b)kJmol﹣1
科目:高中化学 来源: 题型:
【题目】相同状况下混合下列气体,所得混合气体平均摩尔质量为36 g.mol -1 ,它们可能是
A. NO2 和NO B. CO和CH4 C. N2 和O2 D. O2 和CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D 4种短周期元素,它们的元素原子序数依次增大,由B、C、D形成的离子具有相同的电子层结构.B原子的最外层电子数是次外层的三倍,C、D单质都能跟水剧烈反应,1mol D单质跟水反应产生11.2L(标准状况)A气体,此时D转化为具有氖原子核外电子层结构的离子.试填写:
(1)用电子式表示A和C形成化合物的过程 .
(2)C原子的结构示意图 , 写出A、B两元素按1:1原子个数比形成化合物的电子式 .
(3)这4种元素的原子半径由大到小的顺序为 . (用元素符号表示)
(4)写出C单质与水反应的化学反应方程式;.
(5)写出D单质与水反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O(g)=H2O(l) △H=-Q1kJ·mol-1
C2H5OH(g)=C2H5OH(l) △H=-Q2kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H=-O3kJ·mol-1,若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为
A. Q1+Q2+Q3 B. 0.5(Q1+Q2+Q3)
C. 1.5Q1-0.5Q2+0.5Q3 D. 0.5Q1-1.5Q2+0.5Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是
A. 1L1mol·L-1的NaHS溶液中含有HS-的数目小于NA
B. 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA
C. 1mo1C2H4和C3H6的混合气体中含有的碳原子数为2NA
D. 10gH218O含有的中子数为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL
B.45mL
C.30mL
D.15mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定某种矿质元素是否是植物的必需元素,应采用的方法是
A. 检测正常叶片中该矿质元素的含量
B. 分析根系对该矿质元素的吸收过程
C. 分析环境条件对该植物吸收矿质元素的影响
D. 观察在完全培养液中去掉该矿质元素前后植株的生长发育状况
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com