
【题目】足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL
B.45mL
C.30mL
D.15mL
【答案】A
【解析】解:完全生成HNO3 , 则整个过程中HNO3反应前后没有变化,即Cu失去的电子都被O2得到了
根据得失电子守恒:n(Cu)×2=n(O2)×4
n(Cu)×2= ![]() mol×4
mol×4
n(Cu)=0.15mol
所以 Cu(NO3)2为0.15mol
根据
a | ~ | 2OH﹣ |
0.15mol | n(OH﹣) |
则NaOH 为 0.15mol×2=0.3 mol
则NaOH 体积V= ![]() =
= ![]() =0.06L,即 60 ml,
=0.06L,即 60 ml,
故选A.
根据电子得失守恒,求出参加反应的铜,然后求出 Cu(NO3)2 , 再根据 Cu(NO3)2与NaOH 反应的关系,求出NaOH 的物质的量,最终求出NaOH溶液的体积.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A、C原子的L能层中都有两对未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对的电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号________,该能层具有的原子轨道数为_________。
(2)E2+离子的价层电子排布图是__________,F原子的电子排布式是__________。
(3)A元素的最高价氧化物对应的水化物中心原子采用的轨道杂化方式为______,B元素的气态氢化物的VSEPR模型为___________。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们的结构相似,DAB-的电子式为_____________
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为________________________
(6)某种化合物由D、E、F三种元素组成,其晶胞如图所示,其化学式为_____。
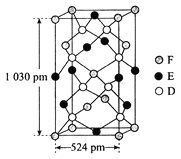
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水作氧化剂的是( )
A. SO3+H2O→H2SO4 B. 2K+2H2O→2KOH+H2↑
C. 2F2+2H2O → 4HF+O2 D. 2Na2O2+2H2O→ 4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2═P4O10 . 已知断裂下列化学键需要吸收的能量分别为:P﹣P akJmol﹣1、P﹣O b kJmol﹣1、P═O c kJmol﹣1、O═O d kJmol﹣1
根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )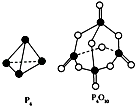
A.(6a+5d﹣4c﹣12b)kJmol﹣1
B.(4c+12b﹣6a﹣5d)kJmol﹣1
C.(4c+12b﹣4a﹣5d)kJmol﹣1
D.(4c+5d﹣4c﹣12b)kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每年3月22日为“世界水日”,2017年活动宣传主题为“落实绿色发展理念,全面推行河长制”,以下做法符合这一主题的是( )
A. 使用含磷洗衣粉 B. 大量开采地下水
C. 工业废水经过处理后排放 D. 垃圾直接倒入河流
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在298K、1.01×105 Pa下,将22g CO2通入750mL 1mol/L NaOH溶液中充分反应,测得反应放出x kJ的热量.已知在该条件下,1mol CO2通入1L 2mol/L NaOH溶液中充分反应放出y kJ的热量.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式是( )
A.CO2(g)+NaOH(aq)═NaHCO3(aq)△H=﹣(2y﹣x)kJ/mol
B.CO2(g)+NaOH(aq)═NaHCO3(aq)△H=﹣(2x﹣y)kJ/mol
C.CO2(g)+NaOH(aq)═NaHCO3(aq)△H=﹣(4x﹣y)kJ/mol
D.2CO2(g)+2NaOH(l)═2NaHCO3(l)△H=﹣(8x﹣2y)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素的叙述,不正确的是( )
A. 碳元素是最基本的元素
B. Ca、Fe、Zn、Cu等微量元素虽然含量不到体重的千万分之一,但是对人的健康却起着重要作用
C. 核酸中的N元素存在于碱基中
D. 组成细胞的元素在非生物界都可以找到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有1mol HNO3的稀硝酸分别与不同质量的铁粉,所得氧化产物a、b与铁粉物质的量关系如图所示.下列有关判断正确的是( ) 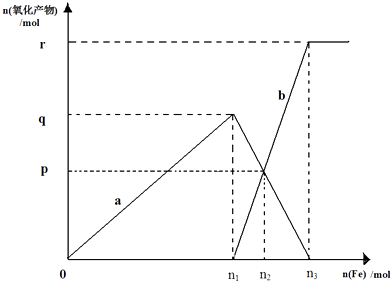
A.a是Fe(NO3)2
B.n1=0.375
C.p=0.20
D.n2=0.30
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式____________________________________。
(2)己知反应N2+3H2![]() 2NH3 △H=akJ/mol。试根据下表中所列键能数据估算a的数值为______。
2NH3 △H=akJ/mol。试根据下表中所列键能数据估算a的数值为______。
化学键 | H-H | N-H | N≡N |
键能kJ/mol | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
己知:C(s,石墨)+O2(g)=CO2(g) △Hl=-393. 5kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
2C2H2(g) +5O2(g) =4CO2(g) +2H2O(1) △H3=-2599kJ/mol
裉推盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应热化学方程式:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com