
【题目】某合作学习小组讨论辨析以下说法 ,其中说法正确的是
①纯碱和熟石灰都是碱;②沼气和水蒸气都是可再生能源;
③冰和干冰既是纯净物又是化合物;④硫酸和食醋既是化合物又是酸;
⑤不锈钢和目前流通的硬币都是合金;⑥粗盐和酸雨都是混合物。
A.③⑤⑥ B.②④⑥ C.①③⑤ D.①②③⑥
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.原电池是化学电源的雏形
B.判断一种电池的优劣主要是看其负极的活泼性
C.依据原电池的原理设计出了化学电源
D.氧化还原反应所释放的化学能是化学电源的能量来源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烯烃与氢气加成后得到2,2-二甲基戊烷,烯烃的名称是
A. 2,2-二甲基-3-戊烯 B. 2,2-二甲基-4-戊烯
C. 4,4-二甲基-2-戊烯 D. 2,2-二甲基-2-戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g) ![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________热反应,且m+n______p (填“>”、“=”或“<”) 。
(2)减压时,A的质量分数__________。(填“增大”、“减小”或“不变”,下同)
(3)若容积不变加入B,则B的转化率__________。
(4)若升高温度,则平衡时B、C的浓度之比将__________。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________;而维持容器内压强不变,充入氖气时,混合物颜色 。(填“变深”、“变浅”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:硫酸铜溶液中滴入氨基乙酸钠(H2N﹣CH2﹣COONa)即可得到配合物A.其结构如图1:
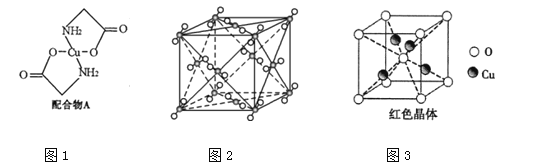
(1)Cu元素基态原子的外围电子排布式为 。
(2)元素C、N、O的第一电离能由大到小排列顺序为 。
(3)配合物A中碳原子的轨道杂化类型为 。
(4)1mol氨基乙酸钠(H2N﹣CH2﹣COONa)含有σ键的数目为 。
(5)氨基乙酸钠分解产物之一为二氧化碳,其结构如图2,它属于________晶体,每个CO2分子与________个CO2分子紧邻。写出二氧化碳的一种等电子体: (写化学式)。
(6) 已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图3,则该化合物的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 由非金属元素组成的化合物不可能是离子化合物
B. 金属原子与非金属原子之间也可以形成共价键
C. 离子化合物中可能含有共价键
D. 共价化合物中不可能含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的下列叙述中,正确的是
A. 离子化合物不可能含共价键 B. 共价化合物可能含离子键
C. 离子化合物中只含离子键 D. 共价化合物中不含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图1所示。其中温度为T1时平衡混合气体中氨气的体积分数为25.0%。
①当温度由T1变化到T2时,平衡常数关系K1 K2(填“>”,“<”或“=”),焓变△H 0。(填“>”或“<”)
②该反应在T1温度下5.00min达到平衡,这段时间内N2的化学反应速率为 。
③T1温度下该反应的化学平衡常数K1= 。
(2)根据最新“人工固氮”的研究报道,在常温常压和光照条件下N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)=4NH3(g)+3O2(g),此反应的△S 0(填“>”或“<”)。若已知:N2(g)+3H2(g)=2NH3(g)△H=a kJ/mol 2H2(g)+O2(g)=2H2O(l)△H=b kJ/mol 2N2(g)+6H2O(l)=4NH3(g)+3O2(g)的△H= (用含a、b的式子表示)。
(3)科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图2所示,则阴极的电极反应式是 。
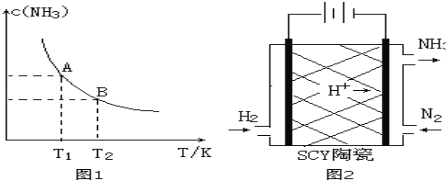
(4)已知某些弱电解质在水中的电离平衡常数(25℃)如下表:
弱电解质 | H2CO3 | NH3.H2O |
电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Kb=1.77×10-5 |
现有常温下0.1 mol·L-1的(NH4)2CO3溶液,
①该溶液呈 性(填“酸”、“中”、“碱”),原因是 。
②该(NH4)2CO3溶液中各微粒浓度之间的关系式不正确的是 。
A.c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3.H2O)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol/L
D.c(NH4+)+c(NH3.H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
E.c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)+c(NH3.H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | HCl ②________ | ③________ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥的后面。
(2)写出实验室由⑩制备O2的化学方程式:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com