
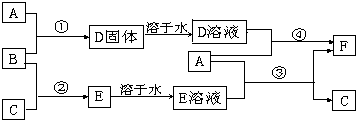
分析 A是用途最广的金属,则A为Fe;D溶液中滴加KSCN溶液显红色,则D中含有铁离子,B、C是常见的气体单质,E溶液为常见强酸,则B为Cl2,C为H2,E为HCl,D为FeCl3,F为FeCl2,据此解答.
解答 解:A是用途最广的金属,则A为Fe;D溶液中滴加KSCN溶液显红色,则D中含有铁离子,B、C是常见的气体单质,E溶液为常见强酸,则B为Cl2,C为H2,E为HCl,D为FeCl3,F为FeCl2.
(1)根据上述推断可知,B为Cl2,F为FeCl2,
故答案为:Cl2;FeCl2;
(2)铁在一定条件下与水蒸气反应生成Fe3O4和氢气,反应的化学方程式为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,第④步反应为Fe与氯化铁反应生成氯化亚铁,离子反应方程式为2Fe3++Fe=3Fe2+,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;2Fe3++Fe=3Fe2+;
(3)F为FeCl2,其溶液中滴入NaOH溶液反应生成氢氧化亚铁白色沉淀,最终被氧化为红褐色的氢氧化铁沉淀,观察到现象为:先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色,
故答案为:先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色;
(4)根据上述分析,D为FeCl3,将FeCl3的饱和溶液滴加到沸水中可以制得氢氧化铁胶体,该反应的化学反应方程式为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,
故答案为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(5)根据上述推断,F为FeCl2,224mL氯气的物质的量为0.01mol,在100mL的FeCl2 的溶液中通入标准状况Cl2 0.01mol,FeCl2溶液恰好转化成FeCl3 溶液,发生反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,则原FeCl2 溶液的物质的量浓度为0.02mol÷0.1L=0.2mol•L-1,
故答案为:0.2mol•L-1.
点评 本题考查无机物的推断、常见化合物的性质、胶体的制备、物质的量浓度的计算等知识,比较基础,注意对元素化合物性质掌握.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
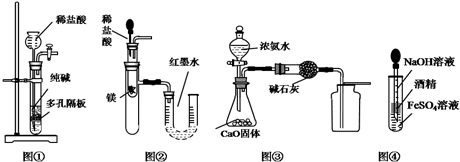
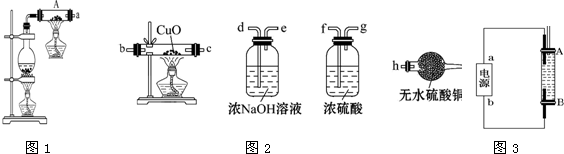
| A. | 用图①所示装置制取少量纯净的CO2气体 | |
| B. | 用图②所示装置验证镁和盐酸反应的热效应 | |
| C. | 用图③所示装置制取并收集干燥纯净的NH3 | |
| D. | 用图④装置制备Fe(OH)2并能保证较长时间观察到白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电过程是化学能转化为电能的过程 | |
| B. | 充电时阳极反应:Ni(OH)2-e-+OH-═NiOOH+H2O | |
| C. | 放电时负极附近溶液的酸性增强 | |
| D. | 放电时电解质溶液中的OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
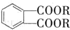 (代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示:
(代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示: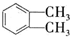 $→_{①光照}^{Cl_{2}}$[A]$\stackrel{②}{→}$[B]$→_{③△}^{Cu、O_{2}}$[C]$\stackrel{④}{→}$[D]$→_{⑤ROH/△}^{浓硫酸}$[DMP]
$→_{①光照}^{Cl_{2}}$[A]$\stackrel{②}{→}$[B]$→_{③△}^{Cu、O_{2}}$[C]$\stackrel{④}{→}$[D]$→_{⑤ROH/△}^{浓硫酸}$[DMP]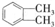 的名称1,2-二甲苯(或邻二甲苯),C中官能团的名称为醛基,DMP的分子式为C10H10O4.
的名称1,2-二甲苯(或邻二甲苯),C中官能团的名称为醛基,DMP的分子式为C10H10O4.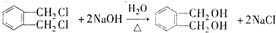 .
. .
.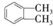 制备DMP的另一种途径:
制备DMP的另一种途径: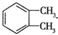 $→_{O_{2}①}^{催化剂、△}$
$→_{O_{2}①}^{催化剂、△}$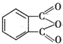 $→_{F②}^{适当条件}$[DMP]
$→_{F②}^{适当条件}$[DMP]查看答案和解析>>
科目:高中化学 来源: 题型:填空题
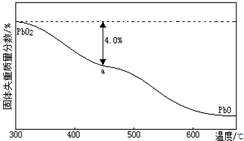 (1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O.PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为PbO+ClO-=PbO2+Cl-.
(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O.PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为PbO+ClO-=PbO2+Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
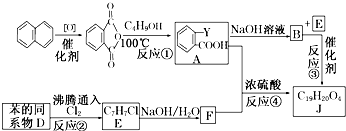
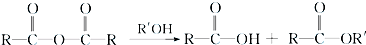
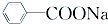 +RCl→
+RCl→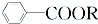 +NaCl;
+NaCl; .
. .
.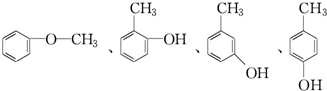 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
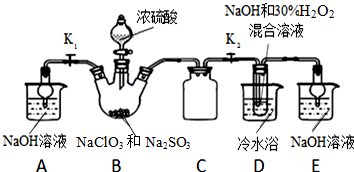
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com