
| A、依据其结构判断该含氧酸为强酸 |
| B、O原子是sP3杂化 |
| C、该分子为直线型非极性分子 |
| D、该分子的电子式是H:O:Cl |
| 1 |
| 2 |
| 1 |
| 2 |
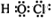 ,故D错误;
,故D错误;

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
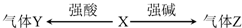 X、Y、Z均为中学化学常见物质,在一定条件下,X能与强酸或强碱溶液发生如图的反应(部分反应物、生成物及反应条件略去).则下列说法不正确的是( )
X、Y、Z均为中学化学常见物质,在一定条件下,X能与强酸或强碱溶液发生如图的反应(部分反应物、生成物及反应条件略去).则下列说法不正确的是( )| A、若X为金属单质,则Y、Z可能为同一物质 |
| B、若X为盐,则Y在标况下的密度一定是1.96g?L-1 |
| C、若X为盐,则Z一定能使湿润的红色石蕊试纸变蓝 |
| D、若X为正盐,则其水溶液中水的电离程度比同温度下纯水的电离程度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.15mol/L |
| B、0.10mol/L |
| C、0.25mol/L |
| D、0.50mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
| B、11.2L Cl2通入足量的NaOH溶液中,转移的电子数为0.5NA |
| C、难失电子的原子,得电子的能力一定强 |
| D、在氧化还原反应中,有一种元素被氧化,肯定有另一种元素被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Fe3+、NH
| ||
B、K+、H+、SO
| ||
C、Fe2+、Fe3+、Na+、NO
| ||
D、Fe2+、NH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、②③④⑤ |
| C、①②④⑤ | D、①②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、羰基硫的电子式为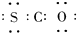 |
| B、羰基硫分子的中心原子为氧 |
| C、羰基硫中三个原子处于同一直线上 |
| D、羰基硫是非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通式相同的不同物质一定属于同系物 |
| B、在相同条件下,燃烧等物质的量的C2H4和C2H5OH,消耗的O2体积相等 |
| C、相对分子质量相同的不同物质一定是同分异构体 |
| D、分子内有苯环和羟基的化合物一定是酚类 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com