
| A、分液操作时,分液漏斗中下层液体从下端放出,上层液体从上口倒出 |
| B、某固体中加入稀盐酸,产生无色无味且能使澄清石灰水变浑浊的气体,证明该固体中一定含有CO32- |
| C、向待测溶液中先加入BaCl2溶液,产生白色沉淀,再加入足量盐酸,沉淀不溶解,证明溶液中一定含有SO42- |
| D、用浓硫酸配制一定物质的量浓度的稀硫酸时,将浓硫酸稀释后,应冷却至室温后再转移到容量瓶中 |


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
| A、XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY |
| B、XYZ3是一种微溶于水的盐,且Y与Z可形成共价化合物化合物YZ或YZ2 |
| C、XYZ3是一种易溶于水的盐,且X与Z可形成离子化合物XZ |
| D、XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、硫酸溶液中加入等物质的量氢氧化钡溶液:Ba2++SO42-+OH-+H+=BaSO4↓+H2O |
| C、往澄清石灰水通入过量二氧化碳气体:CO2+OH-=HCO3- |
| D、在醋酸溶液中加入氧化钠:CH3COOH+O2-=CH3COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧元素的质量比为1:1 |
| B、SO2和SO3的质量比为1:1 |
| C、原子总数之比为1:1 |
| D、分子数之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此陨石是一种纯度较高的硅酸盐矿石 |
| B、此陨石具有耐酸碱的特性 |
| C、陨石中含有游离态的铁是因为在外太空中铁的活性比地球上铁的活性低 |
| D、橄榄石中Fe为+2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
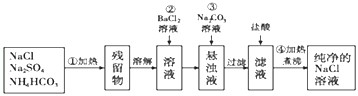
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
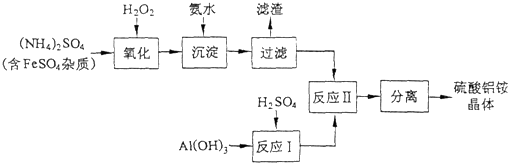
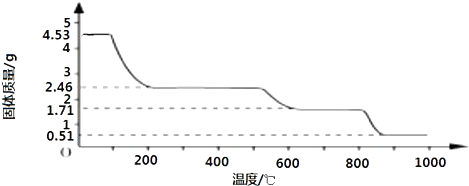
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com