
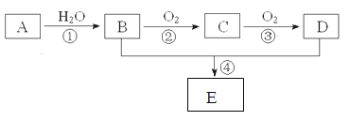
【题目】已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
请回答下列问题:(电子式和化学方程式书写每空2分,其余每空1分)
(1)写出A的电子式 ,B、D分子中的官能团名称分别是 、 。
(2)写出下列反应的化学方程式,并注明反应类型:
① , ;
② , ;
④ , 。
【答案】(1) ![]() 羟基, 羧基 (2)①CH2=CH2 +H2O
羟基, 羧基 (2)①CH2=CH2 +H2O![]() CH3CH2OH;加成反应;
CH3CH2OH;加成反应;
②2CH3CH2OH+O2![]() 2CH3CHO + 2H2O;氧化反应;
2CH3CHO + 2H2O;氧化反应;
④CH3COOH + CH3CH2OH![]() CH3COOCH2CH3+H2O ;取代反应或酯化反应
CH3COOCH2CH3+H2O ;取代反应或酯化反应
【解析】
试题分析:已知A的产量通常用来衡量一个国家的石油化工水平,则A是乙烯,乙烯和水发生加成反应生成乙醇,则B是乙醇。乙醇发生催化氧化生成乙醛,则C是乙醛,乙醛被氧气氧化生成乙酸,则D是乙酸。乙酸和乙醇发生酯化反应生成乙酸乙酯,则E是乙酸乙酯,乙酸乙酯具有果香味。
(1)乙烯含有共价键,电子式为![]() ,乙醇分子中含有羟基,乙酸分子中羧基。
,乙醇分子中含有羟基,乙酸分子中羧基。
(2)根据以上分析可知反应①是乙烯与水的加成反应,方程式为CH2=CH2 +H2O![]() CH3CH2OH;
CH3CH2OH;
反应②是乙醇的催化氧化,方程式为2CH3CH2OH+O2![]() 2CH3CHO + 2H2O;
2CH3CHO + 2H2O;
反应④是酯化反应,方程式为CH3COOH + CH3CH2OH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】下图为甲烷晶体的晶胞结构,下列有关说法正确的是( )
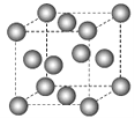
A.甲烷晶胞中的球体只代表一个碳原子
B.晶体中1个![]() 分子有12个紧邻的甲烷分子
分子有12个紧邻的甲烷分子
C.![]() 晶体熔化时需克服共价键
晶体熔化时需克服共价键
D.一个甲烷晶胞中含有8个![]() 分子
分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池板材料除单晶硅外,还有氮、硼、硒、钛、钴、钙等元素组成的化学物质。
(1)钙原子基态时的电子排布式为___________,金属钴堆积方式与镁相似,都属于六方最密堆积,其配位数是___________。
(2)氮元素的第一电离能在同周期中(稀有气体除外)从大到小排第___________位;写出与NO3-互为等电子体的一种非极性分子的化学式___________。
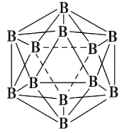
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),其中有两个原子为10B,其余为11B,则该结构单元有___________种不同的结构类型。已知硼酸(H3BO3)为一元弱酸,解释其为一元弱酸的原因____________________________________________。硼酸的结构与石墨相似,层内的分子以氢键相连,含lmol硼酸的晶体中有___________mol氢键。
(4)硒是动物体必需的营养元素。SeO2是硒的重要化合物,SeO2的价层电子对互斥模型是___________。
(5)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为TiCl3·6H2O的晶体,该晶体中两种配体的物质的量之比为1︰5,则该配离子的化学式为___________。
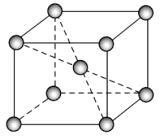
(6)钴晶体的一种晶胞是一种体心立方结构(如图所示),若该晶胞的边长为am,密度为ρg/cm3,NA表示阿伏加德罗常数的值,则钴的相对原子质量可表示为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA 为阿伏加德罗常数的值。下列说法正确的是
A.2.24L(标准状况下)甲苯在O2中完全燃烧,得到0.7NA个CO2分子
B.1mo1乙酸(忽略挥发损失)与足量的C2H518OH浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5分子
C.14g乙烯和丙烯混合气体中的氢原子数为2NA
D.常温常压下,78g苯含有σ键数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分:
C | N | O | F | ||
Si | P | S | Cl | ||
Ge | As | Se | Br | ||
Sn | Sb | Te | I | ||
Pb | Bi | Po | At | ||
![]() 阴影部分元素的外围电子排布式的通式为____。Sb的元素名称为____。基态P原子中,电子占据的最高能级符号为____,该能层具有的原子轨道数为____。
阴影部分元素的外围电子排布式的通式为____。Sb的元素名称为____。基态P原子中,电子占据的最高能级符号为____,该能层具有的原子轨道数为____。
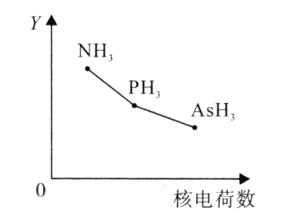
![]() 氮族元素氢化物
氮族元素氢化物![]() 、
、![]() 、
、![]() 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物![]() 性质可能有____。
性质可能有____。
A.稳定性
B.沸点
C.![]() 键能
键能
D.分子间作用力
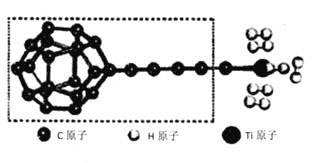
![]() 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。
![]() 和
和![]() 、
、![]() 及
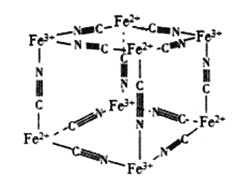
及![]() 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元![]() 未标出
未标出![]() ,该图是普鲁士蓝的晶胞吗?____
,该图是普鲁士蓝的晶胞吗?____![]() 填“是”或“不是”
填“是”或“不是”![]() ,平均每个结构单元中含有____个
,平均每个结构单元中含有____个![]() 。
。
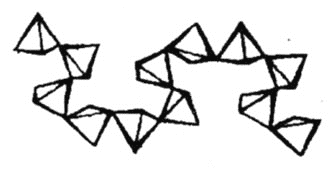
![]() 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是![]() 四面体,多磷酸盐中是
四面体,多磷酸盐中是![]() 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____。
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人体内不可或缺的微量元素,其配合物的研究也是当今科研的重点之一。
![]() 基态Fe原子的价层电子轨道表达式为________________________________;同周期元素中,基态原子的未成对电子数比Fe多的元素为________
基态Fe原子的价层电子轨道表达式为________________________________;同周期元素中,基态原子的未成对电子数比Fe多的元素为________![]() 填元素符号
填元素符号![]() 。
。
![]() 常温下,五羰基铁
常温下,五羰基铁![]() 为黄色液体,其晶体类型为________________;CO与
为黄色液体,其晶体类型为________________;CO与![]() 互为等电子体,二者中沸点较高的是________,原因为________________________。
互为等电子体,二者中沸点较高的是________,原因为________________________。
![]() 普鲁士蓝的化学式为
普鲁士蓝的化学式为![]() ,碳原子与
,碳原子与![]() 形成配位键,其中提供孤电子对的是________
形成配位键,其中提供孤电子对的是________![]() 填元素符号
填元素符号![]() ,
,![]() 中碳原子的杂化方式为________,1mol普鲁士蓝中所含
中碳原子的杂化方式为________,1mol普鲁士蓝中所含![]() 键的数目为________________。
键的数目为________________。
![]() 邻羟基苯甲醛
邻羟基苯甲醛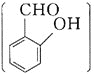 和对羟基苯甲醛
和对羟基苯甲醛 均能与
均能与![]() 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为________________________________________________________。
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为________________________________________________________。
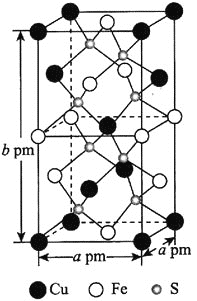
![]() 某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为________________,晶胞中距离Fe原子最近的S原子有________个,若阿伏加德罗常数的值为
某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为________________,晶胞中距离Fe原子最近的S原子有________个,若阿伏加德罗常数的值为![]() ,则该晶体的密度为________________________
,则该晶体的密度为________________________![]() 用含有
用含有![]() 、a、b的代数式表示
、a、b的代数式表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2在工业生产和食品加工等行业用途广泛。某化学小组对SO2的一些性质和反应进行探究。回答下列问题:
I.为探究SO2和Na2O2的反应产物,进行如下实验。
(1)提出假设。假设一:反应产物为Na2SO3和O2;假设二:反应产物为___(填化学式)。
(2)实验验证。
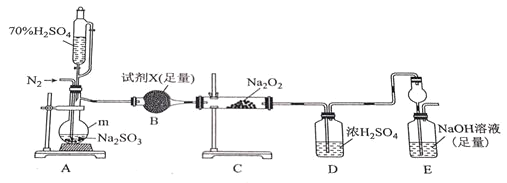
①m的名称为___。
②A中若用稀硫酸代替70%的硫酸,不足之处为___。
③试剂X不宜选择___(填选项字母)。
a.生石灰 b.CaCl2 c.硅胶 d.P2O5
④B的作用___。
II.SO2可以用作葡萄酒的抗氧化剂和防腐剂。该小组同学通过下列操作测定某葡萄酒样品SO2的总含量:量取V1mL样品,加入足量稀H2SO4;将生成的SO2全部蒸出并用足量NaOH溶液吸收;调节溶液的pH后,用cmol/L的标准I2溶液滴定至终点,消耗标准液的体积为V2mL。
(3)滴定反应的离子方程式为___;样品中的总含量为___mg/L(用含c,V1,V2的代数式表示)。
(4)若用足量稀盐酸代替稀H2SO4,会导致所测SO2的总含量___(填偏高偏低或无影响)。
III.(5)设计实验证明H2SO3的酸性强于H2CO3:___。(供选试剂:NaHCO3溶液、CO2、SO2、KMnO4(H+)溶液、NaOH溶液、澄清石灰水)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对有机物性质进行探究,下列描述不正确的是
A.对甲基苯甲醛(![]() )能使酸性高锰酸钾溶液褪色,说明它含有醛基
)能使酸性高锰酸钾溶液褪色,说明它含有醛基
B.将铜丝在酒精灯的外焰上加热变黑后再移至内焰,铜丝又恢复到原来的红色
C.向2mL10%的NaOH溶液中滴几滴CuSO4溶液,再加入乙醛溶液加热有红色沉淀产生
D.向苯酚溶液中滴加几滴稀溴水出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的同分异构体数目与分子式为C3H6Cl2的同分异构体数目相同的是
A.![]() B.C8H8O2(含苯环且属于酸)
B.C8H8O2(含苯环且属于酸)
C.C3H8O2D.C7H8O(含苯环)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com