
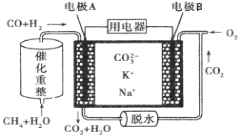
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )
A.反应CH4+H2O![]() 3H2+CO,每消耗1mol CH4转移12mol电子
3H2+CO,每消耗1mol CH4转移12mol电子
B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C.电极B上发生的电极反应为:O2+2CO2+4e-=2![]()
D.电池工作时,![]() 向电极B移动
向电极B移动
【答案】C
【解析】
燃料电池中通入氧气侧为正极,通入燃料侧为负极,则A为负极,B为正极。
A.反应CH4+H2O![]() 3H2+CO中碳元素由CH4中的-4价升高到CO中的+2价,被氧化,CH4和H2O中的氢元素由+1价降低为H2中的0价,被还原,则反应中每消耗lmol CH4转移6mol 电子,A项错误;
3H2+CO中碳元素由CH4中的-4价升高到CO中的+2价,被氧化,CH4和H2O中的氢元素由+1价降低为H2中的0价,被还原,则反应中每消耗lmol CH4转移6mol 电子,A项错误;
B.根据示意图可知电池中不存在OH-,氢气参与的电极反应式为:H2-2e-+CO32-=H2O+CO2,B项错误;
C.B为正极,氧气得电子,结合CO2生成![]() ,电极反应式为O2+2CO2+4e-=2
,电极反应式为O2+2CO2+4e-=2![]() ,C项正确;
,C项正确;
D.根据B项、C项分析可知B电极产生![]() ,A电极消耗
,A电极消耗![]() ,因此
,因此![]() 由电极B(正极)向电极A(负极)移动,D项错误;
由电极B(正极)向电极A(负极)移动,D项错误;
故选C。


科目:高中化学 来源: 题型:
【题目】
人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、二氧化碳、青霉素、硝酸钾、乙醇、氨等“分子”改变过人类的世界。
(1)铁原子在基态时,外围电子排布式为__________________________。
(2)1 mol CO2分子中含有σ键的物质的量为_________________________。
(3)6-氨基青霉烷酸的结构如图所示:
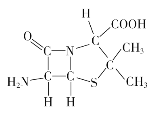
①其中C、N、O电负性由小至大的顺序是_________________。
②其中碳原子的杂化类型是______________。
(4)硝酸钾中![]() 的空间构型为___________,写出
的空间构型为___________,写出![]() 的一种等电子体的化学式______________。
的一种等电子体的化学式______________。
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是_____________。
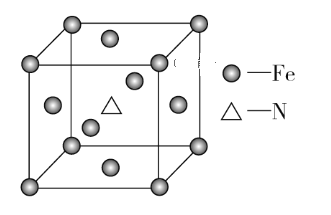
(6)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,该晶体的化学式为____________,若两个最近的Fe原子间的距离为a cm,则该晶体的密度为_________g·cm-3。(用NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4NO3 溶液受热可发生分解反应:NH4NO3![]() N2↑+HNO3+H2O(未配平)。用 NA 表示阿伏加德罗数的值,下列说法正确的是
N2↑+HNO3+H2O(未配平)。用 NA 表示阿伏加德罗数的值,下列说法正确的是
A.分解时每生成 2.24 L(标准状况)N2,转移电子的数目为 0.6NA
B.2.8 g N2 中含有共用电子对的数目为 0.3NA
C.56 g Fe 与足量稀硝酸反应生成 NO2 分子的数目为 3NA
D.0.1 mol·L-1 NH4NO3 溶液中,NH4+的数目小于 0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的有机物充分燃烧,产物先通入浓硫酸,浓硫酸增重5.4 g,然后通入足量澄清石灰水中,完全吸收后,经过滤得到20 g沉淀,则该有机物可能是( )
A. 乙醇B. 乙烯C. 甲酸甲酯D. 乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)物质X的产量通常用来衡量一个国家的石油化工水平。以X为主要原料合成重要的有机化合物路线如下图所示,请回答下列问题。

(1)X所含官能团的名称是______________,A物质所含官能团的名称是________。
(2)反应③的化学方程式是_______________,以乙烯为原料可合成有机高分子化合物D,反应①的化学方程式是____________________,该反应属于______反应(填有机反应类型)。
(3)下列物质中,不能通过乙烯加成反应得到的是________(填序号)。
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
(4)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是______。
②实验开始时,试管b中的导管不伸入液面下的原因是______。
③反应结束后,将试管b中的混合液经过____(填写实验分离操作)可得到纯净的乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,发现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
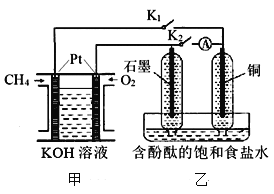
A. 断开K2,闭合K1时,石墨电极上的电极反应式为:2 H++ 2e-=H2↑
B. 断开K1,闭合K2时,铜电极上的电极反应式为:Cl2 + 2e-=2Cl-
C. 甲装置属于燃料电池,该电池正极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
D. 甲烷燃料电池的总电极反应式为:CH4+2O2 +2NaOH=Na2CO3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
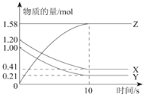
A.反应的化学方程式为: X(g)+Y(g)![]() Z(g)
Z(g)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.温度、体积不变,10s时充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式不正确的是
A.NaHCO3在水中的电离方程式:NaHCO3 = Na++HCO![]()
B.氯化镁溶液与氨水反应的离子方程式:Mg2++2OH-= Mg(OH)2↓
C.Cl2与水反应的离子方程式:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
D.醋酸钠水解的离子方程式CH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C物质为烃类,在标准状况下的密度为1.16g/L,F物质具有水果香味,G物质不能水解。转化关系如图所示,省略了反应条件。

请回答下列问题:
(1)写出G的分子式:____________________。
(2)D中官能团的名称是__________________________。 C→A的反应类型____________
(3)请写出反应B+E→F的化学方程式:______________________。
(4)下列有关说法正确的是_____________________________。
A.C物质燃烧时,易产生大量黑烟 B.物质B和甘油( )互为同系物
)互为同系物
C.一定条件下,A可被直接氧化为D D.用NaOH溶液可以区分B、D、F
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com