
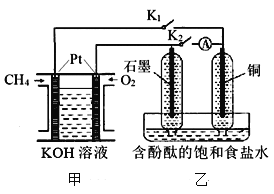
【题目】某兴趣小组设计如下微型实验装置。实验时,发现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
A. 断开K2,闭合K1时,石墨电极上的电极反应式为:2 H++ 2e-=H2↑
B. 断开K1,闭合K2时,铜电极上的电极反应式为:Cl2 + 2e-=2Cl-
C. 甲装置属于燃料电池,该电池正极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
D. 甲烷燃料电池的总电极反应式为:CH4+2O2 +2NaOH=Na2CO3+3H2O
【答案】D
【解析】
实验时,断开K2,闭合K1,乙装置是电解池,石墨作阳极,铜是阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以两极均有气泡产生;一段时间后,断开K1,闭合K2,乙池形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,石墨作正极,氯气得电子发生还原反应。
实验时,断开K2,闭合K1,乙装置是电解池,石墨作阳极,铜是阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以两极均有气泡产生;一段时间后,断开K1,闭合K2,乙池形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,石墨作正极,氯气得电子发生还原反应;
A.断开K2,闭合K1时,该装置是电解池,铜作阴极,石墨作阳极,石墨电极上氯离子失电子发生氧化反应,所以其电极反应式为:2Cl--2e-=Cl2↑,故A错误;
B.断开K1,闭合K2时,该装置是原电池,铜作负极,负极上氢气失电子发生氧化反应,所以铜电极上的电极反应式为:H2-2e-═2H+,故B错误;
C.甲装置属于燃料电池,该电池正极上氧气得电子发生还原反应,该电池正极的电极反应式为O2十2H2O+4e-=4OH-,故C错误;
D.甲装置属于燃料电池,甲烷和氧气、氢氧化钠反应生成碳酸钠和水,所以总电极反应式为:CH4+2O2+2NaOH=Na2CO3+3H2O,故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】
G是功能高分子材料。以甲苯为原料合成G的一种流程如下(部分条件和产物略去)。
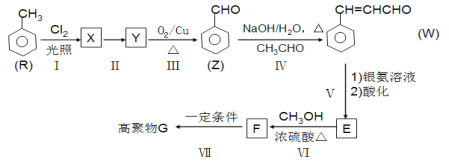
回答下列问题:
(1)W中官能团名称是:_______________________;反应Ⅰ的类型是_________________。
(2)反应Ⅱ的试剂和条件是____________、_______________;Z的名称是______________。
(3)写出F→G的化学方程式:_________________。
(4)T是E的同分异构体,T的苯环上有3个互不相同的取代基,T的结构有______种。
(5)W分子中最多有______个原子共平面。
(6)以乙醇为原料,经过三步合成正丁醇。参照上述流程图设计合成路线。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是( )
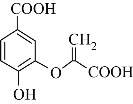
A. 可看成羧酸类、酯类等B. 分枝酸分子中含有3种官能团
C. 分子式为C10H10O 6D. 1mol分枝酸最多可与3molNaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《环境科学》曾刊发我国科研部门采用零价铁活化过硫酸钠(Na2S2O7其中S为+6价)去除废水中的正五价砷的研究成果,其反应机理模型如图,(NA为阿伏加德罗常数的值)下列说法正确的是
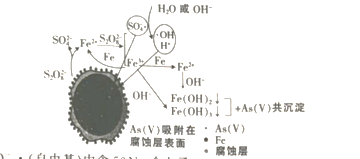
A.1 molSO4-· (自由基)中含50NA个电子
B.pH越大,越不利于去除废水中的正五价砷
C.1 mol过硫酸钠中含NA个过氧键
D.转化过程中,若共有1 mol S2O82-被还原,则参加反应的Fe为56 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )
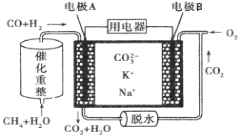
A.反应CH4+H2O![]() 3H2+CO,每消耗1mol CH4转移12mol电子
3H2+CO,每消耗1mol CH4转移12mol电子
B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C.电极B上发生的电极反应为:O2+2CO2+4e-=2![]()
D.电池工作时,![]() 向电极B移动
向电极B移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1 L 0.1 mol·L-1 NH4Cl溶液中,不断加入固体NaOH后,NH![]() 与NH3 · H2O的变化趋势如下图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
与NH3 · H2O的变化趋势如下图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
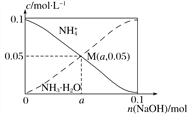
A. 在M点时,n(OH-)-n(H+)=(a-0.05) mol
B. 随着NaOH的加入,![]() 不断增大
不断增大
C. M点溶液中水的电离程度比原溶液小
D. 当n(NaOH)=0.1 mol时,c(OH-)>c(Cl-)-c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲。红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如图所示。
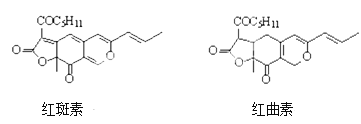
下列说法正确的是
A. 红斑素和红曲素都存在2个手性碳原子
B. 一定条件下红斑素和红曲素都能发生加聚和自身的缩聚反应
C. 红斑素中含有醚键、羰基、酯键这三种含氧官能团
D. 1 mol红曲素最多能与6molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
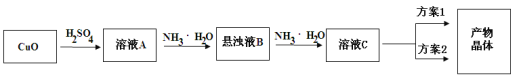
相关信息如下:
①[Cu(NH3)2]SO4·H2O在溶液中存在以下电离(解离)过程:
[Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++SO42-+H2O [Cu(NH3)4]2+ ![]() Cu2++4NH3
Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇、水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如图
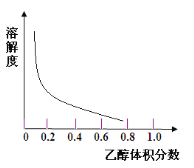
请根据以上信息回答下列问题:
(1)方案1的实验步骤为:a.加热蒸发,b.冷却结晶,c.抽滤,d.洗涤,e.干燥。
①步骤1的抽滤装置如图所示,下列有关抽滤操说法作正确的是_____。
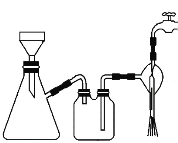
A.完毕后的先关闭水龙头,再拔下导管
B.上图装置中只有一处错误
C.抽滤后滤液可以从上口倒出,也可从支管倒出
D.滤纸应比漏斗内径小且能盖住所有小孔
②该方案存在明显缺陷,因为得到的产物晶体中往往含有_____杂质,产生该杂质的原因是______。
(2)方案2的实验步骤为:a.向溶液C中加入适量____,b.抽滤,c.洗涤,d.干燥。
①请在上述空格内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是________。
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
洗涤的具体操作是:____________。
③步骤d采用________干燥的方法。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜晶体(CuSO4·![]() H2O蓝色)在110℃开始失去结晶水,150℃失去全部结晶水,生成白色的无水硫酸铜。依据硫酸铜晶体受热失去结晶水的事实,可以设计硫酸铜晶体水含量
H2O蓝色)在110℃开始失去结晶水,150℃失去全部结晶水,生成白色的无水硫酸铜。依据硫酸铜晶体受热失去结晶水的事实,可以设计硫酸铜晶体水含量![]() 的测定方法。请根据以下实验数据回答相关问题:(M(CuSO4)=159.5g/mol、M(H2O)=18.0g/mol)
的测定方法。请根据以下实验数据回答相关问题:(M(CuSO4)=159.5g/mol、M(H2O)=18.0g/mol)
坩埚质量 | 坩埚和晶体的质量 | 完全失去结晶水后坩埚和剩余固体的质量 |
11.685g | 13.691g | 12.948g |
(1)要完成此实验,至少要称量______次。
(2)![]() ______(保留2位小数),本次实验结果____(填“偏高”、“偏低”)。
______(保留2位小数),本次实验结果____(填“偏高”、“偏低”)。
(3)造成本次误差可能的原因是______。
A. 加热时有晶体溅出
B. 实验前坩埚内有受热不挥发、不分解也不与硫酸铜反应的杂质
C. 粉末未完全变白就停止加热
D. 加热后放在空气中冷却
(4)请写出造成本次误差还有可能存在的其他原因(写出其中一点)_____________________。
(5)如果硫酸铜晶体样品不纯,测定结果________。
A.没有偏差 B. 一定偏小 C. 一定偏大 D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com