
【题目】硫代硫酸钠俗称保险粉,可用于照相业作定影剂、纸浆漂白作脱氯剂等。实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。本实验对Na2S纯度要求较高,利用图1所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按图1所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,抽滤。将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
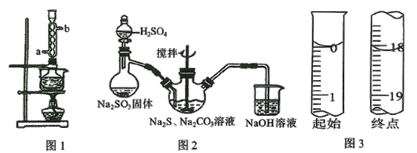
(1)下列说法不正确的是____________。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用冷水淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
E.在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析出而损失、去除杂质
(2)用图2所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是_________,三颈烧瓶中发生反应的化学方程式____。
(3)保险粉样品中Na2S2O3·5H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6。准确称取W g样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000 mol·L-1碘的标准溶液进行滴定。请回答:
①到达滴定终点的标志______________。
②滴定起始和终点的液面位置如图3,则消耗碘的标准溶液体积为__________mL,产品的纯度为______________(设Na2S2O3·5H2O相对分子质量为M)。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的纯度的测量结果___________(填“偏高”、“偏低”或“不变”)。
(4)某研究小组以硫代硫酸钠与硫酸反应来探究外界条件对反应速率的影响,设计实验如下:
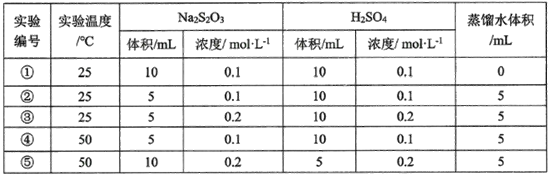
下列有关说法不正确的是__________
A.该同学在实验中采用的研究方法是实验比较法
B实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
C.实验①和③溶液变浑浊的时间相同
D.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
【答案】AD 蒸馏烧瓶 2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2 溶液变为蓝色,且30s内不恢复原色 18.10 ![]() 偏低 CD
偏低 CD
【解析】
(1)A、硫化钠在常温时溶解度较小,若用冷水淋洗,不能溶解硫化钠,故A错误;
B、抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸,故B正确;
C、常温时,硫化钠溶解度小,杂质能溶于乙醇,且乙醇易挥发,所以洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体,故C正确;
D、如果高温烘干,硫化钠被空气中的氧化,故D错误;
E、在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析出而损失、去除杂质,E正确;
故选AD;
(2)、盛放Na2SO3固体的玻璃仪器名称是蒸馏烧瓶;三颈烧瓶中发生反应的化学方程式:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2;
(3)①用配制的碘溶液滴定硫代硫酸钠,滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色,说明反应到达终点,故答案为:滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色;
②终点读数为18.10mL,起点读数为0.00mL,故消耗碘的标准溶液体积为18.10mL;滴定时消耗碘的物质的量![]() ,根据反应方程式可知Na2S2O3的物质的量为3.62×10-3mol,Na2S2O3的质量为
,根据反应方程式可知Na2S2O3的物质的量为3.62×10-3mol,Na2S2O3的质量为![]() ,故纯度为
,故纯度为![]() ;
;
③局部变色就停止滴定,消耗标准溶液体积偏小,会使样品中Na2S2O3·5H2O的纯度的测量结果偏低,故答案为:偏低;
(4)A、该同学在实验中采用的研究方法是实验比较法,故A正确;
B、实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响,故B正确;
C、实验①和③浓度不相同,所以溶液变浑浊的时间也不相同,故C错误;
D、其他条件不变时,探究温度对化学反应速率的影响,应选择实验②和④,故D错误;
故选CD。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】金属镁在点燃条件下与二氧化碳反应:2Mg+CO2![]() 2MgO+C。当0.4mol Mg与0.1mol CO2充分反应后,物质的种类及其数量正确的是( )
2MgO+C。当0.4mol Mg与0.1mol CO2充分反应后,物质的种类及其数量正确的是( )
A.0.2 mol MgO + 0.1 molC
B.0.4 mol MgO + 0.2 molC
C.0.3 mol Mg + 0.2 mol MgO +0.1mol C
D.0.2 mol Mg + 0.2 mol MgO+0.1 molC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL则该R摩尔质量为___。
(2)已知CO、SO2的混合气体质量共18.4g,标准状况下体积为8.96L,则可推知该混合气体中CO的物质的量分数为____,混合气体的平均相对分子质量为____。
(3)同温同压下,SO2与氢气的密度之比为____;若体积相同时,两种气体的质量比为____。
(4)质量比为51∶28的NH3、CO所含质子数之比为____。
(5)标准状况下,aL气体X2和bL气体Y2恰好完全反应生成cL气体Z,若2a=6b=3c,则Z的化学式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列说法正确的是
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:a>b>c
B.KNO3溶液和CH3OOONH4溶液pH均为7,但两溶液中水的电离程度不相同
C.5.0×10-3 mol·L-1KHA溶液的pH=3.75,该溶液中c(A2-)<c(H2A)
D.己知某分散系中存在:M(OH)2(s)![]() M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液的pH等于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在474.8g水中溶解25.2g草酸晶体(H2C2O4·2H2O,相对分子质量为126),得到一份草酸浓溶液,该溶液密度为2.0g/cm3。
(1)以上过程得到的草酸浓溶液的物质的量浓度为___mol/L。
(2)现需用上述浓溶液配制0.1mol/L的草酸溶液450mL。
①实验中用到的玻璃仪器有胶头滴管、烧杯、量筒、___。
②应量取浓溶液的体积为___mL。
③下列情况中,会导致配制的0.1mol/L的草酸溶液浓度偏高的有___(填字母)。
A.配制浓溶液所使用的草酸晶体失去部分结晶水
B.使用“左码右物”的方法称量草酸晶体
C.容量瓶未经干燥就使用
D.量取浓溶液时仰视刻度线
(3)H2C2O4·2H2O受热易分解,分解产物均为氧化物,其中一种产物能使澄清石灰水变浑浊,请写出H2C2O4·2H2O受热分解的化学方程式___。
(4)用移液管量取10.00mL酸性K2Cr2O7溶液,恰好与20.00mL0.1mol/L的草酸溶液反应,还原产物为Cr3+,氧化产物为CO2。在此实验中,草酸体现___性;此酸性K2Cr2O7溶液的物质的量浓度为___mol/L(保留小数点后2位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关于溶液和胶体的说法正确的是 ( )
A.常温下,向FeCl3溶液滴加NaOH溶液至有红褐色小颗粒生成即可制得![]() 胶体
胶体
B.溶液是均一稳定的,胶体是介稳体系,所以人的肉眼就可以区分开来
C.在![]() 胶体中,逐滴加入稀硫酸至过量,先产生红褐色沉淀后又消失
胶体中,逐滴加入稀硫酸至过量,先产生红褐色沉淀后又消失
D.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图:

请回答下列问题:
(1)实验室只有100mL、250mL、500mL三种规格的容量瓶,但要配制480 mL 0.50 mol/L的稀硫酸,需量取该浓硫酸______mL。
(2)接下来完成此实验你将用到的仪器有20mL量筒、烧杯、玻璃棒、胶头滴管、____________。
(3)使用容量瓶前必须进行的一步操作是____________。
(4)要从所配溶液中取出10 mL稀释至20 mL,则稀释后溶液的物质的量浓度为__________。
(5)下列操作会使所配溶液浓度偏低的是__________。
A. 用量筒量取浓硫酸,读数时仰视刻度线
B. 转移溶液时未洗涤烧杯
C. 定容时俯视容量瓶的刻度线
D. 定容摇匀后,发现液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质]
继密胺树脂/石墨烯量子点复合微球新型白光发光材料后,2019年8月13日中国科学院福建物质结构研究所合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料![]() 并获得了该化合物的LED器件。
并获得了该化合物的LED器件。
(1)基态O原子能量最高的电子,其电子云在空间有______个延展方向;C原子的基态电子排布式为______;
(2)![]() 与
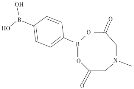
与![]() 互为等电子体,构型为_______;苯-1,4-二硼酸甲基亚氨基二乙酸酯结构如图所示,硼原子和氮原子的杂化方式分别为__________、__________。
互为等电子体,构型为_______;苯-1,4-二硼酸甲基亚氨基二乙酸酯结构如图所示,硼原子和氮原子的杂化方式分别为__________、__________。
(3)石墨的熔点大于金刚石的熔点,试分析原因:________。
(4)![]() 可用
可用![]() 检验,其对应的酸有两种,分别为硫氰酸(HSC≡N)和异硫氰酸(HN=C=S),这两种酸中沸点较高的是____________,试分析原因:_________;热稳定性:
检验,其对应的酸有两种,分别为硫氰酸(HSC≡N)和异硫氰酸(HN=C=S),这两种酸中沸点较高的是____________,试分析原因:_________;热稳定性:![]() _______(填“<”“>”或“=”)
_______(填“<”“>”或“=”)![]() 。
。
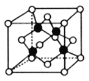
(5)超高热导率半导体材料——砷化硼(BAs)晶胞结构如图所示(As位于体内,B位于顶点和面心),已知晶胞参数为a pm,阿伏加德罗常数的值为![]() ,As原子到B原子最近距离为________(用含a的式子表示),该晶体的密度是_______g.cm-3 (列出含a、
,As原子到B原子最近距离为________(用含a的式子表示),该晶体的密度是_______g.cm-3 (列出含a、![]() 的计算式即可)。
的计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茉莉花香气的成分有多种,有机物E (C9H10O2)是其中的一种,它可以从茉莉花中提取,也可以用酒精和苯的某一同系物(C7H8)为原料进行人工合成,合成路线如下:
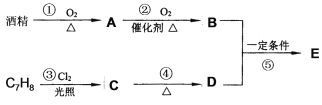
【1】C物质中官能团的名称是:___________。
【2】③的有机反应类型是:_______________。
【3】反应④发生还需要的试剂是:_____________。
【4】写出反应⑤的化学方程式:______________。
【5】证明反应②中A物质己完全转化为B物质的方法是:________________。
【6】E的同分异构体中,苯环上只有一个取代基,并包含一个酯基的结构有多个,下面是其中2个的结构简式:
![]() 、
、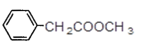
请再写出2个符合上述要求的E的同分异构体结构简式:______和__________
【7】请写出以CH2=CHCH2CH3为唯一有机原料制备CH2=CHCH=CH2的合成路线(无机试剂任选)________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com