
【题目】下列有关烷烃的叙述中,不正确的是
A. 在烷烃分子中,所有的化学键都为单键
B. 所有的烷烃在光照条件下都能与氯气发生取代反应
C. 烷烃分子的通式为CnH2n+2,符合该通式的烃不一定是烷烃
D. 随着碳原子的增加,烷烃的熔、沸点逐渐升高。
科目:高中化学 来源: 题型:
【题目】[化学一选修3:物质结构与性质]
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对立的辐射波长为_____________nm(填序号)。
A.589.2 B.500.3 C.650.2 D.434.4
(2)K和Fe属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Fe低,原因是________________________。
(3)基态I原子中,核外电子占据最高能层的符号为_____________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长a=0.446am,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示,K与O间的最短距离为________nm,与K紧邻的O个数为_____________________。

(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于________位置,O处于__________位置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol有机物A(分子式为C6H10O4)经水解得1mol B和2mol C,C经分子内脱水得D,D可发生加聚反应生成 ![]() ,由此可知A为( )
,由此可知A为( )
A.HOOC(CH2)4COOH
B.HOOC(CH2)3COOCH3
C.CH3COO(CH2)2COOCH3
D.CH3CH2OOC﹣COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列中和反应对应的离子方程式能以“H++OH-═H2O”表示的是
A.醋酸和氢氧化钠溶液反应B.氢氧化镁和盐酸反应
C.澄清石灰水和硝酸反应D.氢氧化钡和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是 。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在 范围。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K= 。
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式: 。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是 (只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用 方法。
TiCl4 | SiCl4 | |
熔点/℃ | -25.0 | -68.8 |
沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.活化分子碰撞即发生化学反应
B.升高温度会加快反应速率,原因是增加了活化分子的碰撞次数
C.某一反应的活化分子百分数是个定值
D.活化分子的碰撞不一定是有效碰撞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能合有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉定生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示。下列叙述错误的是
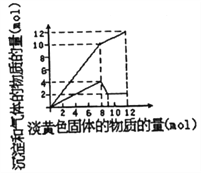
A. 溶液中一定含有的离子是NH4+、Al3+和Mg2+
B. 溶液中肯定不含有Cu2+,可能含有Fe2+
C. 所加的淡黄色固体是Na2O2
D. 溶液中的NH4+和Al3+的物质的量浓度之比3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
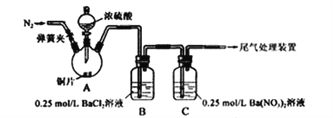
实验操作和现象:
操作 | 现象 |
关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(1)A中反应的化学方程式是_________________;
(2)C中生成白色沉淀的离子方程式为__________________;
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。为证实各自的观点,在原实验基础上,甲、乙两同学分别作了如下实验:甲在原有操作之前通N2,一段时间,B中产生大量白色沉淀。乙在A、B间增加盛放饱和NaHSO3溶液的洗气瓶,B中有少量白色沉淀。产生少量沉淀的原因是_____________。
(4)结合(3)中两同学的实验现象。你认为原实验B中产生大量白色沉淀的主要原因是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com