
【题目】某溶液中可能合有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉定生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示。下列叙述错误的是
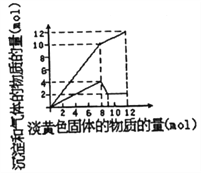
A. 溶液中一定含有的离子是NH4+、Al3+和Mg2+
B. 溶液中肯定不含有Cu2+,可能含有Fe2+
C. 所加的淡黄色固体是Na2O2
D. 溶液中的NH4+和Al3+的物质的量浓度之比3:1
【答案】B
【解析】A.淡黄色固体加入溶液中,并加热溶液时,有刺激性气体放出和白色沉淀生成,则淡黄色固体为Na2O2,图象实际为两个图合在一起,较上的是气体,较下的是沉淀,图象中加入8mol过氧化钠后,沉淀减小,且没有完全溶解,则溶液中一定没有Fe2+和Cu2+,一定有Mg2+、NH4+、Al3+,加入8mol过氧化钠之后,生成气体减小,故加入8mol过氧化钠时,铵根离子完全反应,A正确;B.根据以上分析可知B错误;C.根据以上分析可知C正确;D.根据图像可知溶解氢氧化铝消耗过氧化钠是1mol,1mol过氧化钠产生2mol氢氧化钠,根据Al(OH)3+OH-=AlO2-+2H2O可知氢氧化铝是2mol,所以铝离子是2mol。8mol过氧化钠产生4mol氧气,所以产生的氨气是10mol-4mol=6mol,则铵根是6mol,所以溶液中的NH4+和Al3+的物质的量浓度之比3:1,D正确,答案选B。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】为了探究铁、铜及其化合物的性质,某同学设计并进行了下列两组实验。
实验一:
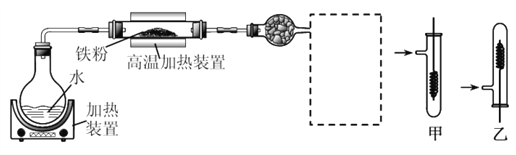
已知:3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
(1)虚线框处宜选择的装置是________(填“甲”或“乙”);实验时应先将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净氢气中,观察到的实验现象是______________________。
(2)实验后,为检验硬质玻璃管中的固体是否含+3价的铁元素,该同学取一定量的固体并用一定浓度的盐酸溶解,滴加_______溶液(填试剂名称或化学式),没有出现血红色,说明该固体中没有+3价的铁元素。请你判断该同学的结论是否正确并说明理由_________________。
实验二:
绿矾是含有一定量结晶水的硫酸亚铁,为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A 称重,记为m2 g,B为干燥管。按下图连接好装置进行实验。
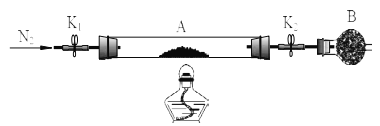
实验步骤如下:(1)________,(2)点燃酒精灯,加热,(3)______,(4)______,(5)______,
(6)称量A, 重复上述操作步骤,直至 A 恒重,记为m3 g。
(3)请将下列实验步骤的编号填写在对应步骤的横线上
a.关闭 K1 和 K2 b.熄灭酒精灯 c.打开 K1 和 K2 缓缓通入 N2 d.冷却至室温
(4)必须要进行恒重操作的原因是_________________。
(5)已知在上述实验条件下,绿矾受热只是失去结晶水,硫酸亚铁本身不会分解, 根据实验记录,
计算绿矾化学式中结晶水数目 x=__________________(用含 m1、 m2、 m3的列式表示)。
【答案】 乙 铜丝由黑变红 硫氰化钾或 KSCN 不正确,因为铁过量时: Fe+2Fe3+→3Fe2+ c b d a 确保绿矾中的结晶水已全部失去 ![]()
【解析】试题分析:实验一:(1)铁与水蒸气反应生成Fe3O4和氢气,虚线框中的装置是用氢气还原氧化铜的装置,根据氢气的密度比空气小分析;氧化铜被氢气还原为铜单质;(2)Fe3+能使KSCN溶液变成血红色;单质铁能把Fe3+还原为Fe2+;
实验二:(3)由于装置中含有空气,空气能氧化硫酸亚铁,所以加热前要排尽装置中的空气,利用氮气排出空气,为使生成的水蒸气完全排出,应该先熄灭酒精灯再关闭K1 和 K2;冷却后再称量;(4)进行恒重操作可以确保绿矾中的结晶水已全部失去;(5)根据题意,生成硫酸亚铁是![]() ,生成水的质量是
,生成水的质量是![]() ,根据
,根据![]() 计算x值;
计算x值;
解析:实验一:(1)铁与水蒸气反应生成Fe3O4和氢气,虚线框中的装置是用氢气还原氧化铜的装置,氢气的密度比空气小,所以用向下排空气法收集氢气,故选乙;氧化铜被氢气还原为铜单质,现象是铜丝由黑变红;(2)Fe3+能使KSCN溶液变成血红色,滴加KSCN溶液检验是否含有Fe3+,若溶液变为血红色,则含有Fe3+;单质铁能把Fe3+还原为Fe2+,当铁过量时: Fe+2Fe3+=3Fe2+,所以没有出现血红色,不能说明该固体中没有+3价的铁元素;
实验二:(3)由于装置中含有空气,空气能氧化硫酸亚铁,所以加热前要排尽装置中的空气,利用氮气排出空气,为使生成的水蒸气完全排出,应该先熄灭酒精灯再关闭K1 和 K2;冷却后再称量,正确的步骤是(1)打开 K1 和 K2 缓缓通入 N2,(2)点燃酒精灯,加热,(3)熄灭酒精灯,(4)冷却至室温,(5)关闭 K1 和 K2,(6)称量A, 重复上述操作步骤,直至 A 恒重,记为m3 g;(4)进行恒重操作可以确保绿矾中的结晶水已全部失去;(5根据题意,生成硫酸亚铁是![]() ,生成水的质量是
,生成水的质量是![]() ,
,
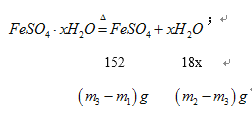
X=![]() 。
。
【题型】实验题
【结束】
24
【题目】PTT 是一种高分子材料,具有优异性能,能作为工程塑料、纺织纤维和地毯等材料而得到广泛应用。其合成路线可设计为:
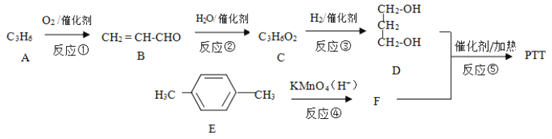
已知: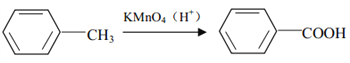
(1)B 中所含官能团的名称为_________,反应②的反应类型为_________。
(2)反应③的化学方程式为_________。
(3)写出 PTT 的结构简式_________。
(4)某有机物X 的分子式为C4H6O,X与B互为同系物,写出X可能的结构简式_________。
(5)请写出以 CH2=CH2 为主要原料(无机试剂任用)制备乙酸乙酯的合成路线流程图(须注明反应条件)。(合成路线常用的表示方式为:![]() )____________
)____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关烷烃的叙述中,不正确的是
A. 在烷烃分子中,所有的化学键都为单键
B. 所有的烷烃在光照条件下都能与氯气发生取代反应
C. 烷烃分子的通式为CnH2n+2,符合该通式的烃不一定是烷烃
D. 随着碳原子的增加,烷烃的熔、沸点逐渐升高。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软质隐形眼镜材料W、树脂X的合成路线如图所示. 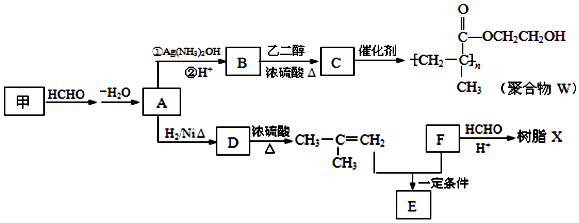
已知: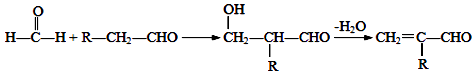
(1)A中含有的官能团的结构简式是 .
(2)甲的结构简式是 .
(3)B→C反应的化学方程式是 .
(4)B有多种同分异构体.属于酯且含有碳碳双键的同分异构体共有种(不考虑顺反异构.
(5)已知F的相对分子质量为110,1molF可与足量钠反应生成22.4L氢气(标准状况下),
苯环上的氢原子化学环境都相同.则F还能发生的反应是(填序号)
a.加成反应 b.氧化反应 c.加聚反应 d.水解反应
(6)写出树脂X可能的结构简式(写出一种即可).
(7)E的分子式为C10H14O2 , 含三个甲基,苯环上的一溴代物有两种,生成E的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是常见的氧化剂、催化剂和活性电极材料。
(1)工业上,以惰性材料为电极,电解MaSO4溶液(含少量稀硫酸)制备MnO2。写出阳极的电极反应式:_________________________________。
(2)已知如下热化学方程式(K代表平衡常数):
①MnCO3(s)![]() Mn0(s)+CO2(g)△H1 K1
Mn0(s)+CO2(g)△H1 K1
②2MnO(s)+O2(g)![]() 2MnO2(s)△H2 K2
2MnO2(s)△H2 K2
③2MnCO3(n)+O2(g)![]() 2MnO2(s)+2CO2(g)△H3 K3
2MnO2(s)+2CO2(g)△H3 K3
△H3=________用△H1,△H2表示);K3=________用K1、K2表示)。
(3)反应②在低温条件下能自发进行,则△H3________0(填“>"“<"或“=")。
(4)在密闭容器中投入足量的MnCO3,一定条件下发生反应MnCO3(s)![]() MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
①温度、压强对MnCO3分解率的影响如图所示:
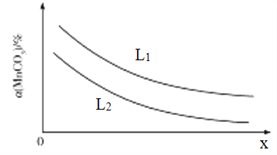
比较:L1__________L2(填“>"“<”或“=")。
②保持温度不变,将容器休积扩大至原来的2倍,则ρ(CO2)的变化范围是____________。
③保持温度不变,将容器体积压缩至原来的一半,达到新平衡时下列物理量一定不变的是____(填代号)。
A.平衡常数K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)一定温度下,在容积为2L的恒容密闭容器中加入足量的MnCO3(s)和5molO2,发生反应:2MnCO3(s)+O2(g)![]() 2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A.水的离子积变大、pH变小、呈酸性
B.水的离子积变大、pH变小、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积不变、pH不变、呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的实验现象及结论描述正确的是
A.钠在空气中燃烧发出黄色火焰,生成氧化钠
B.钠加入到CuSO4溶液中,有红色物质析出,即析出Cu单质
C.向CaCl2溶液中通入少量CO2气体,出现白色沉淀,即生成CaCO3固体
D.氢气在氯气中燃烧产生苍白色火焰,生成了HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学实验的叙述正确的是( )
A.用已知浓度的盐酸滴定未知浓度的氨水选用酚酞做指示剂
B.用待测液润洗滴定用的锥形瓶
C.Na2CO3溶液保存在带橡胶塞的试剂瓶中
D.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验事实与原子结构模型建立的关系正确的是
A.阴极射线实验发现电子:道尔顿原子结构模型
B.α粒子散射实验发现原子核:卢瑟福原子结构模型
C.氢原子光谱发现电子分层排布:卢瑟福原子结构模型
D.α粒子散射实验发现电子:汤姆生原子结构模型
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com