
��һ��������ܱ������У��������»�ѧ��Ӧ�� CO2(g)��H2(g ) CO(g)��H2O(g)���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
CO(g)��H2O(g)���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
| T/��C | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
(1)�÷�ӦΪ________��Ӧ(����ȡ������ȡ�)��
(2)���жϸ÷�Ӧ�Ƿ��Ѵﻯѧƽ��״̬��������________��
a��������ѹǿ���� b�����������c(CO)����
c��v��(H2)��v��(H2O) d����������ƽ���ܶȲ���
(3)ij�¶��£���2 L���ܱ������У�����1 mol CO2��1 mol H2��ַ�Ӧ��ƽ��ʱ��CO��ƽ��Ũ��Ϊ0.25 mol��L��1�����жϴ�ʱ���¶�Ϊ________�档
(4)����(3)�������¶��£���1 L���ܱ������У�����2 mol CO2��3 mol H2��ַ�Ӧ��ƽ��ʱ��H2�����ʵ���Ϊ________��
a������1.0 mol����b������1.0 mol c������0.5 mol����d����ȷ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C����ѧ�������ֵ��ʣ�A��B��C������ ����֮��ķ�Ӧ��ϵ��ͼ91��ʾ������B��D��E��F��ˮ��Һ�����ԡ���D��C��E��F�ҳ�����ֻ��BΪ��̬����A��B��C�ֱ�Ϊ(����)
����֮��ķ�Ӧ��ϵ��ͼ91��ʾ������B��D��E��F��ˮ��Һ�����ԡ���D��C��E��F�ҳ�����ֻ��BΪ��̬����A��B��C�ֱ�Ϊ(����)
A��Fe��Cl2��Cu B��Fe��Cl2��H2
C��Cu��Cl2��Fe D��Fe��Cl2��Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�������淴Ӧ����
A��CO2��H2O��H2CO3��H2CO3��CO2��H2O��������


|
 2H2����O2����2H2+O2����2H2O
2H2����O2����2H2+O2����2H2O 
 C��2SO2��O2 2SO3��2SO3 2SO2��O2����
C��2SO2��O2 2SO3��2SO3 2SO2��O2����
D��H2��I2 �� 2HI��2HI �� H2��I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶��£��ڹ̶��ݻ����ܱ������У����淴ӦA(g)��3B(g) 2C(g)�ﵽƽ��ʱ�����A�� B�� C���ʵ���֮��Ϊ2:2:1���������¶Ȳ��䣬��2:2:1�����ʵ���֮���ٳ���A��B��C�������ж���ȷ���ǣ� ��
2C(g)�ﵽƽ��ʱ�����A�� B�� C���ʵ���֮��Ϊ2:2:1���������¶Ȳ��䣬��2:2:1�����ʵ���֮���ٳ���A��B��C�������ж���ȷ���ǣ� ��
A��ƽ�����淴Ӧ�����ƶ� B��ƽ�ⲻ�ᷢ���ƶ�
C���õ������������� D���õ�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ij��ѧ��Ӧ��ƽ�ⳣ������ʽΪ 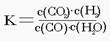 �� �ڲ�ͬ���¶��¸÷�Ӧ��ƽ
�� �ڲ�ͬ���¶��¸÷�Ӧ��ƽ
�ⳣ�����±���
| t �� | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
�����й���������ȷ����(����)
A���÷�Ӧ�Ļ�ѧ����ʽ��CO(g)��H2O(g) CO2(g)��H2(g)
CO2(g)��H2(g)
B��������Ӧ������Ӧ�Ƿ��ȷ�Ӧ
C������1 L���ܱ�������ͨ��CO2��H2��1 mol,5 min���¶����ߵ�830 �棬��ʱ���CO2Ϊ0.4 mol���÷�Ӧ�ﵽƽ��״̬
D����ƽ��Ũ�ȷ��Ϲ�ϵʽ �����ʱ���¶�Ϊ1 000 ��
�����ʱ���¶�Ϊ1 000 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڻ�ѧ����˵����ȷ���ǣ� ��
A.ֻ�����ڷ���֮�� B.ֻ����������֮��
C.����ԭ��֮���ǿ����� D.���ۼ�ֻ�ܴ����ڹ��ۻ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪A��ԭ��������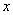 ��
��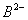 ��
��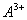 ������ͬ�ĵ��Ӳ�ṹ����BԪ�ص�ԭ������Ϊ�� ��
������ͬ�ĵ��Ӳ�ṹ����BԪ�ص�ԭ������Ϊ�� ��
A. 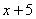 B.
B. 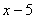 C.
C. 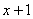 D.
D. 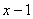
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
25��ʱ����֪����ĵ��볣����K(CH3COOH) = 1.8 ��10��5��K1(H2CO3) = 4.4 ��10��7��K2(H2CO3) = 4.7 �� 10��11��K(HClO) = 4.0 ��10��8��������˵����ȷ����
A��������ˮ��̼�����Ʋ���Ӧ
B��25��ʱ��0.1mol/L�Ĵ�����Һ��0.01mol/L�Ĵ�����Һ�У�Kaǰ��С�ں���
C��NaClO��Һ��ͨ������������̼�ķ�ӦΪ��2NaClO+CO2+ H2O = Na2CO3 +2HClO
D�������ʵ���Ũ�ȵ�̼������Һ����������Һ������������Һ��pH
pH(Na2CO3)��pH(NaClO)��pH(CH3COONa)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ����������յõ��Ĺ�������Ϊ���ѧʽ��
��1����K2CO3��Һ����____________________________
��2����Na2SO3��Һ����___________________________
��3����AlCl3��Һ���ɲ�����_______________________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com