
【题目】为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外.将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口.充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液.试回答:
(1)写出铜片溶于稀硝酸的离子方程式
(2)吹入空气前小试管中的现象是铜片逐渐溶解.溶液变蓝色及
(3)假设小试管中加入了 0.192g铜片和5ml浓度为2mol/L的稀硝酸,则充分反应后小试管内溶 液中NO ![]() 物质的量浓度为mol/L(忽略溶液体积变化).
物质的量浓度为mol/L(忽略溶液体积变化).
(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,试写出该反应的离子方程式
(5)将等质里的铜片分别与等体积过量的浓、稀硝酸反应(假设溶液体积不变 所得溶液前者呈绿色,后者呈蓝色.某同学认为可能是Cu2浓度的差异引起的,你认为是否正确?(填“正确”或“不正确”),理由是 .
【答案】
(1)3Cu+8H++2NO ![]() =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
(2)有红棕色气体生成
(3)1.6
(4)2NO2+2OH﹣=NO ![]() +NO
+NO ![]() +H2O
+H2O
(5)不正确;等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓度相等
【解析】解:(1)铜和稀硝酸反应的离子方程式为:3Cu+8H++2NO ![]() =3Cu2++2NO↑+4H2O,所以答案是:3Cu+8H++2NO3﹣=3Cu2++2NO↑+4H2O;(2)吹入空气前小试管中的现象是铜片逐渐溶解,铜和稀硝酸反应生成硝酸铜溶液为蓝色溶液,生成一氧化氮气体和大试管中远期反应生成二氧化氮红棕色气体,所以答案是:有红棕色气体生成;(3)铜和稀硝酸反应的离子方程式为:3Cu+8H++2NO
=3Cu2++2NO↑+4H2O,所以答案是:3Cu+8H++2NO3﹣=3Cu2++2NO↑+4H2O;(2)吹入空气前小试管中的现象是铜片逐渐溶解,铜和稀硝酸反应生成硝酸铜溶液为蓝色溶液,生成一氧化氮气体和大试管中远期反应生成二氧化氮红棕色气体,所以答案是:有红棕色气体生成;(3)铜和稀硝酸反应的离子方程式为:3Cu+8H++2NO ![]() =3Cu2++2NO↑+4H2O,0.192g铜片物质的量=
=3Cu2++2NO↑+4H2O,0.192g铜片物质的量= ![]() =0.003mol,5ml浓度为2mol/L的稀硝酸溶液中硝酸物质的量=0.005L×2mol/L=0.01mol,反应的硝酸根离子物质的量为0.002mol,剩余硝酸根离子物质的量=0.01mol﹣0.002mol=0.008mol,则溶液中硝酸根离子浓度=
=0.003mol,5ml浓度为2mol/L的稀硝酸溶液中硝酸物质的量=0.005L×2mol/L=0.01mol,反应的硝酸根离子物质的量为0.002mol,剩余硝酸根离子物质的量=0.01mol﹣0.002mol=0.008mol,则溶液中硝酸根离子浓度= ![]() =1.6mol/L,所以答案是:1.6;(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,是二氧化氮自身氧化还原反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:2NO2+2OH﹣=NO
=1.6mol/L,所以答案是:1.6;(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,是二氧化氮自身氧化还原反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:2NO2+2OH﹣=NO ![]() +NO
+NO ![]() +H2O, 所以答案是:2NO2+2OH﹣=NO
+H2O, 所以答案是:2NO2+2OH﹣=NO ![]() +NO
+NO ![]() +H2O;(5)等质量的铜片与等体积过量的浓、稀硝酸反应,硝酸足量,则Cu完全反应,铜离子浓度相同,所以颜色不同与Cu2+浓度的差异引起的说法不正确,所以答案是:不正确;等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓度相等.
+H2O;(5)等质量的铜片与等体积过量的浓、稀硝酸反应,硝酸足量,则Cu完全反应,铜离子浓度相同,所以颜色不同与Cu2+浓度的差异引起的说法不正确,所以答案是:不正确;等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓度相等.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. SO3与SO2 B. BF3与NH3 C. BeCl2与SCl2 D. H2O与SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现.这是因为通气后混和液中产生的ClO﹣被H2O2还原,发生激烈反应,产生能量较高的氧分子,然后立即转变为普通氧分子,多余的能量以红光放出.本实验所用的仪器及导管如图1所示. 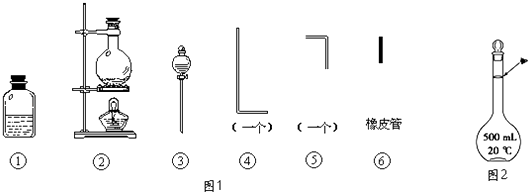
根据要求填写下列空白:
(1)组装氯气发生装置时,应选用的仪器及导管为(填写图中编号).
(2)本实验进行时,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次为 .
(3)仪器①的橡皮塞上至少应有2个孔的原因是 .
(4)本实验需配置10molL﹣1的NaOH溶液500mL,用到的仪器除了托盘天平、烧杯外,还须用到的仪器有(填仪器名称),定容时操作如图2,则所配溶液浓度(填“偏高”或“偏低”).
(5)实验时仪器①中ClO﹣与H2O2反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两支惰性电极插入CuSO4溶液中,通电电解,当有 1 mol 的 OH-放电时,溶液显浅蓝 色,则下列叙述正确的是
A. 阳极上析出11.2 L O2(标准状况)
B. 阴极上析出 32 g Cu
C. 阴极上析出11.2 L H2(标准状况)
D. 阳极和阴极质量都无变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10﹣羟基喜树碱的结构如图所示.下列关于10﹣羟基喜树碱的说法正确的是( ) 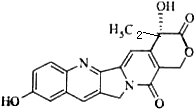
A.分子式为C20H16N2O5
B.不能与FeCl3溶液发生显色反应
C.不能发生酯化反应
D.一定条件下,1mol该物质最多可与1mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: 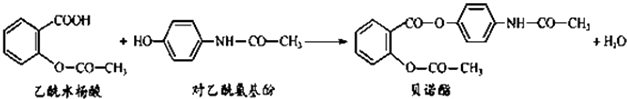
下列有关叙述正确的是( )
A.贝诺酯分子中有三种含氧官能团
B.对乙酰氨基酚核磁共振氢谱中共有四个峰
C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3 溶液反应
D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)请写出下列反应对应的离子方程式: ①用盐酸中和氢氧化钠溶液: .
②用稀硫酸清洗铁锈(Fe2O3):;
(2)写出离子反应方程式所对应的一个化学方程式.①Ba2++2OH﹣+SO ![]() +2H+=BaSO4↓+2H2O
+2H+=BaSO4↓+2H2O
②CO ![]() +2H+=H2O+CO2↑ .
+2H+=H2O+CO2↑ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如下反应,总结规律,然后完成下列问题:①Al(OH)3+H2OAl(OH) ![]() +H+;
+H+;
②NH3+H2ONH ![]() +OH﹣
+OH﹣
(A)已知B(OH)3是一元弱酸,试写出其电离方程式________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象.可以通过下列装置所示实验进行探究.下列说法正确的是( ) 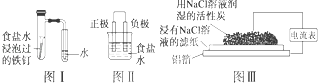
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl﹣由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl﹣﹣2e﹣═Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3 , 生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com