
【题目】如图所示是组成细胞的主要元素及其比例,根据所示信息回答下列问题:

(1)构成细胞的主要元素有______________。
(2)组成生物体的最基本元素占细胞总量的______。
(3)在组成细胞的元素中,基本元素为____________,其在细胞鲜重情况下,百分比从多到少依次为______________;在细胞干重情况下,其占细胞干重百分比从多到少依次为_____________ 。
(4)组成细胞的元素大多以 _______ 的形式存在,一类是_________,另一类是_________。
【答案】C H O N P S 18% C H O N O>C>H>N C> O>N>H 化合物 有机化合物 无机化合物
【解析】
1、组成生物体的化学元素根据其含量不同分为大量元素和微量元素两大类。
(1)大量元素是指含量占生物总重量万分之一以上的元素,包括C、H、O、N、P、S、K、Ca、Mg,其中C、H、O、N为基本元素,C为最基本元素,O是含量最多的元素;
(2)微量元素是指含量占生物总重量万分之一以下的元素,包括Fe、Mn、Zn、Cu、B、Mo等。
2、化合物包含有机化合物和无机化合物。
(1)由图可知,构成细胞的主要元素有C、H、O、N、P、S。
(2)组成生物体的最基本元素是C,占细胞总量的18%。
(3)在组成细胞的元素中,基本元素为C、H、O、N,其在细胞鲜重情况下,百分比从多到少依次为O>C>H>N;在细胞干重情况下,其占细胞干重百分比从多到少依次为C> O>N>H。
(4)组成细胞的元素大多以化合物的形式存在,一类是有机化合物,另一类是无机化合物。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中有关物质的量浓度关系正确的是( )
A. 0.1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
B. NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)
C. 室温下,由pH=1的CH3COOH溶液与pH=13的NaOH溶液等体积混合,溶液中离子浓度大小的顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D. 常温下,在pH=8的NaA溶液中:c(Na+)-c(A-)=9.9×10-7 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
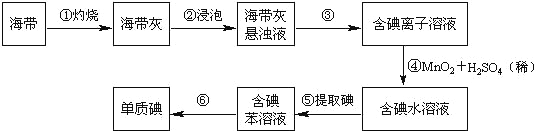
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_______(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_______;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_______。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是_______。在分液操作中,应充分振荡,然后静置,待分层后______(填标号),以下略。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) ![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别为
2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45 mol·L-1·min-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1 ④v(D)=0.45 mol·L-1·s-1,该反应进行的快慢顺序为
A. ④>③=②>① B. ④<③=②<① C. ①>②>③>④ D. ④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q是合成防晒霜的主要成分,某同学以石油化工的基本产品为主要原料,设计合成Q的流程如下(部分反应条件和试剂未注明):

已知:
I.钯催化的交叉偶联反应原理(R、R1为烃基或其他基团,X为卤素原子):
R—X+R1—CH=CH2![]() R1—CH=CH—R+H—X
R1—CH=CH—R+H—X
II.C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成CO2,其消去产物的分子只有一个碳原子上没有氢原子。
III.F不能与氢氧化钠溶液反应,G的核磁共振氢谱中有3个峰且为对位取代物。
请回答下列问题:
(1)反应⑤的反应类型为_______________,G的结构简式为_________________。
(2)C中官能团的名称是____________________;C8H17OH的名称(用系统命名法命名)为__________________。
(3)X是F的同分异构体,X遇氯化铁溶液发生显色反应且环上的一溴取代物有两种,写出X的结构简式:________________________。
(4)写出反应⑥的化学方程式:______________________________________________。
(5)下列有关B、C的说法正确的是________(填序号)。
a.二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色
b.二者都能与碳酸氢钠溶液反应产生二氧化碳
c.1 mol B或C都能最多消耗44.8 L(标准状况)氢气
d.二者都能与新制氢氧化铜悬浊液反应
(6)分离提纯中间产物D的操作:先用饱和碳酸钠溶液除去C和浓硫酸,再用水洗涤,弃去水层,最终通过__________操作除去C8H17OH,精制得到D。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列性质的比较中,正确的是
A.非金属性:Br>ClB.稳定性:H2S>H2O
C.酸性:H2CO3>HNO3D.碱性:Ca(OH)2>Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据表中的信息回答下列问题
元素 | A | B | C | D | E |
有关信息 | 其原子核内只有1个质子 | 其单质在空气中体积含量最多 | 其原子M层有3个电子 | 食盐中的金属元素 | 单质在常温、常压下是黄绿色的气体 |
(1)D离子的结构示意图:________,B原子的电子式:________,E离子的电子式:________。
(2)和B元素的氢化物所含电子数相同的分子有多种,写出任意2种:________,________。
(3)A元素与E元素组成的化合物的电离方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 25℃、101 kPa下:① 2 Na(s) + 1/2 O2(g) = Na2O(s) △H1 = - 414 kJ / mol
② 2 Na(s) + O2(g) = Na2O2(s) △H2 = - 511 kJ / mol
下列说法正确的是
A. ①和②产物的阴阳离子个数比不相等
B. ①和②生成等物质的量的产物,转移电子数不同
C. 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D. 25℃、101 kPa下,Na2O2(s) + 2 Na(s) = 2 Na2O(s) △H = -317 kJ / mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com