
【题目】①A、B、C、D 4种物质均含有元素X,有的还可能含有元素Y或者Z,元素Y、X、Z为前20号元素且核电荷数依次递增。
②X在A、B、C、D中的化合价分别为0价、-1价、+1价、+5价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
请回答下列问题:
(1)写出元素X、Y、Z的元素符号:X________,Y________,Z________。
(2)写出A、B、C、D的化学式:A________,B________,C________,D________。
(3)写出③中反应的化学方程式________________________。
(4)写出④中反应的化学方程式________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】RFC是一种将水电解技术与氢氧燃料电池技术向结合的可充电电池。下图为RFC工作原理示意图,下列有关说法正确的是
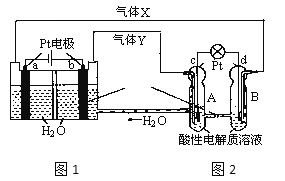
A.图1把化学能转化为电能,图2把电能转化为化学能,水得到了循环使用
B.当有0.1mol电子转移时,a极产生0.56LO2(标准状况下)
C.c极上发生的电极反应是:O2+4H++4e-=2H2O
D.图2中电子从c极流向d极,提供电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法Ⅰ | 用炭粉在高温条件下还原CuO |
方法Ⅱ | 用肼(N2H4)还原新制Cu(OH)2 |
方法Ⅲ | 电解法:2Cu+H2O |
已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H=-akJ·mol-1
C(s)+1/2O2(g)=CO(g);△H=-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s);△H=-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g) △H = kJ·mol-1
(1)工业上很少用方法Ⅰ制取Cu2O是由于方法Ⅰ反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因: 。
(2)方法Ⅱ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,写出电极反应式:阴极 ;阳极 。

(4)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g) ![]() 2H2(g)+ O2(g) ⊿H >0,水蒸气的浓度(mol·L-1)随时间t (min)变化如下表所示:
2H2(g)+ O2(g) ⊿H >0,水蒸气的浓度(mol·L-1)随时间t (min)变化如下表所示:
序号 | Cu2Oa克 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | 方法Ⅱ | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 方法Ⅱ | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | 方法Ⅲ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是 (填字母代号)。
a.实验的温度T2小于T1
b.实验①前20 min的平均反应速率v(O2)=7×10-5 mol·L-1 min-1
c.实验②比实验①所用的催化剂催化效率高
d.实验①、②、③的化学平衡常数的关系:K1=K2<K3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,在一定条件下既能起加成反应,也能起取代反应,但不能使KMnO4酸性溶液褪色的是 ( )
A. 甲烷 B. 苯 C. 乙烯 D. 乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中含有右表离子中的某5种,且其浓度均为0.1mol/L(不考虑水的电离与离子水解)。向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化。下列叙述不正确的是( )

A.X溶液中不可能含有HC03-或CO32-
B.生成无色气体的离子方程式为:3Fe2+ +NO3-+4H+=3Fe3++NO+2H2O
C.根据电荷守恒,原溶液中一定含Mg2+
D.X溶液中一定含3种阳离子、2种阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.钠放入水中 Na+H2O=Na++OH-+H2↑
B.电解饱和食盐水 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.实验室用氯化铝溶液和氨水制氢氧化铝 Al3++3OH-=Al(OH)3↓
D.向碳酸氢铵溶液中加入足量氢氧化钠溶液 HCO3-+OH-=CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家开发出一种新型锂—氧电池,其能量密度极高,效率达90%以上。电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:
O2+4LiI+2H2O2I2+4LiOH

对于该电池的下列说法不正确的是( )
A.放电时负极上I- 被氧化
B.充电时Li+从阳极区移向阴极区
C.充电时阴极反应为LiOH+e-==Li+OH-
D.放电时正极反应为O2+2H2O+4Li++4e-==4LiOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想用SO2制取少量硫酸,其装置如图所示:

①H+移向 极(填“a”或“b”),c极的电极名称是 ,
②a极发生的电极反应式为 。
③c极发生的电极反应式为 。
④标准状况下,A装置吸收3.36LSO2时,B装置中溶液最多减重 g。(装置中气体的溶解性忽)不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.78gNa2O2固体中阴离子的个数为2NA
B.标准状况1.12L氯气与H2O反应,反应中转移的电子数为0.1NA
C.CO2通过Na2O2使其增重ag时,反应中转移的电子数为aNA/56
D.60gSiO2含有的化学键数目为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com