
【题目】下列物质一定属于纯净物的是( )
A. C3H6B. C2H6OC. CHCl3D. C2H4Cl2
科目:高中化学 来源: 题型:
【题目】1,6一己二酸(G)是合成尼龙的主要原料之一,可用烃A氧化制备.制备G的合成路线如图1:
回答下列问题:
(1)化合物A的质谱图如图2,则A的化学名称为 .
(2)C→D的反应类型为 .
(3)F的结构简式为 .
(4)由G合成尼龙的化学方程式为 .
(5)由A通过两步反应制备1,3﹣环己二烯的合成路线为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 苯能使溴水因发生取代反应而褪色,且生成溴苯
B. 甲苯能使酸性高锰酸钾溶液褪色
C. 苯中没有典型的碳碳双键,但能发生加成反应
D. 苯中各原子均在同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把 500 ml 含有 BaCl2和 KCl的混合溶液分成5等份。取一份加入含 a mol碳酸钠的液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A. 0.1(b-2a) molL-1 B. 10(b-2a) molL-1
C. 10(b-a) molL-1 D. 10(2a-b) molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、硫的单质及其化合物在生产、生活中应用广泛,辉铜矿(主要成分是Cu2S)是冶炼铜和制硫酸的重要原料.
(1)已知:①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g)△H=﹣768.2kJmol﹣1 ②2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0kJmol﹣1
则Cu2S(s)+O2(g)=2Cu(s)+SO2(g)△H= .
(2)已知25℃时,KSP(BaSO4)=1.1×1010 , 向仅含0.1molL﹣1 Ba(OH)2的废液中加入等体积0.12molL﹣1硫酸,充分搅拌后过滤,滤液中c(Ba2+)=
(3)上述冶炼过程中会产生大量的SO2 , 回收处理SO2 , 不仅能防止环境污染,而且能变害为宝,回收处理的方法之一是先将SO2转化为SO3 , 然后再转化为H2SO4 . ①450℃时,某恒容密闭容器中存在反应:2SO2(g)+O2(g)2SO3(g)△H<0,下列事实能表明该反应达到平衡的是 .
A.容器内气体密度不变
B.O2、SO2的消耗速率之比为1:2
C.n(SO2):n(O2):n(SO3)=2:1:2
D.容器内压强不再发生变化
②450℃、0.1MPa下,将2.0molSO2和1.0molO2置于5L密闭容器中开始反应,保持温度和容器体积不变,SO2的转化率(α)随着时间(t)的变化如图1所示,则该温度下反应的平衡常数K= . 若维持其他条件不变,使反应开始时的温度升高到500℃,请在图1中画出反应开始到平衡时SO2转化率的变化图象.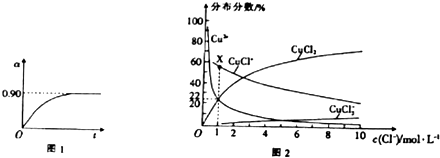
(4)已知CuCl2溶液中,铜元素的存在形式与c(Cl﹣)的相对大小有关,具体情况如图2所示(分布分数是指平衡体系中含铜微粒物质的量占铜元素总物质的量的百分比) ①若溶液中含铜微粒的总浓度为amolL﹣1 , 则X点对应的c(CuCl+)=(用含a的代数式表示).
②向c(Cl﹣)=1molL﹣1的氯化铜溶液中滴入少量AgNO3溶液,则浓度最大的含铜微粒发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组的同学拟利用碘化亚铁与碳酸氢钠的反应来制备高纯度的碘化钠晶体.回答下列问题:
(1)碘化亚铁溶液的制备:将碘和铁粉按物质的量之比在 ![]() ﹣
﹣ ![]() 之间配料,加入三颈烧瓶中(如图),然后加入适量水,并向装置中持续通入N2 , 在40﹣60℃下搅拌反应30﹣50min,待反应完成检验出反应液中不含碘单质后,过滤即制得碘化亚铁溶液. ①配料中铁粉过量的目的是;持续通入N2的目的是 .
之间配料,加入三颈烧瓶中(如图),然后加入适量水,并向装置中持续通入N2 , 在40﹣60℃下搅拌反应30﹣50min,待反应完成检验出反应液中不含碘单质后,过滤即制得碘化亚铁溶液. ①配料中铁粉过量的目的是;持续通入N2的目的是 .
②检验反应液中不含碘单质的方法是 .
(2)碘化钠溶液的制备:将制备好的碘化亚铁溶液加入碳酸氢钠溶液中,控制碘化亚铁与碳酸氢钠的物质的量之比在 ![]() ∽
∽ ![]() ,在80﹣100℃下,反应30﹣50min,反应生成碘化钠及硫酸亚铁等.该反应的化学方程式为 .
,在80﹣100℃下,反应30﹣50min,反应生成碘化钠及硫酸亚铁等.该反应的化学方程式为 .
(3)点化钠的提纯与结晶: ①除去碘化钠溶液中以HCO3﹣的方法是 .
②从碘化钠溶液中获得碘化钠晶体(20℃时溶解度为179/100g水,100℃时溶解度为302/100g水)的操作方法是 .
(4)碘化钠的提度的测定: 该小组同学称取制得的碘化钠晶体18.1g,溶于水后加入50mL2.5mol/LAgNO3溶液,过滤、洗涤、干燥,称得沉淀的质量为28.2g.则碘化钠晶体的纯度为 . (杂质不参与反应,结果保留至小数点后两位)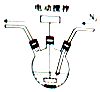
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下。回答下列问题 (注:Na2O2可以与H2O、CO2能反应):
(1)装置Ⅳ中盛放的药品是______________,其作用是__________________________。

(2)若规定气体的气流方向从左到右,则各仪器接口的标号字母(a、b……)顺序是:
空气进入________,________接________,________接________,________接________。
(3)装置Ⅱ的作用_____________________________________________________。
(4)操作中通空气和加热的顺序为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定体积的SO3(g)充入恒容的密闭容器中,发生反应2SO3(g)2SO2(g)+O2(g)并达到平衡;保持温度不变,再充入相同体积的SO3(g),达到新平衡后,与原平衡相比,下列值减小的是( )
A.平均相对分子质量
B.SO3(g)的转化率
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示.钛铁矿主要成分为钛酸亚铁(FeTiO3),其中一部分铁元素在风化过程中会转化为+3价. 
已知:TiOSO4遇水会水解.
(1)步骤②中,用铁粉将Fe3+转化为Fe2+的反应的离子方程式为 .
(2)步骤③中,实现混合物的分离是利用物质的(填字母序号). a.熔沸点差异 b.溶解性差异 c.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是(填操作名称).
(4)请结合化学用语用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理: .
(5)可以利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4 , 易溶于水),该反应的离子方程式为 .
(6)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2﹣CaO作电解质,利用如下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛. 
①写出阳极所发生反应的电极反应式: .
②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com