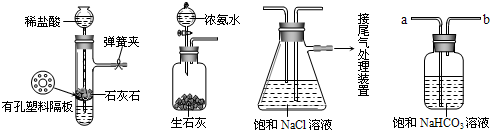
��2010?������һģ����ͼ1Ϊij��ʵ��װ��ʾ��ͼ�����м���װ�úͲ���ҩƷ���Ѿ�ʡ�ԣ�װ�âٺ�װ�â�Ϊ���巢��װ�ã���
��1����ͬѧ������ͼ1��ʾװ�ã���A��B������һʢ��Ũ�����ϴ��ƿ���Ʊ�NO
2����֤�����ʣ�װ�â�����ʵ�����Ʊ�NH
3����װ�â��Ʊ�����O
2��Aװ������ӦҩƷ�ڴ�����ʱ������Ӧ�Ļ�ѧ����ʽ��
��B����ˮ��ȴ��U�����к���ɫ����������Խ�ӽ�U�ܵײ���ɫԽdz�������ԭ��
��Ϊ2NO+O2=2NO2��2NO2�����أ�?N2O4����ɫ��������Ӧ�Ƿ��ȷ�Ӧ��U�ܵײ����¶Ƚ��ͣ�����ƽ�������ƶ���NO2Ũ�Ƚ��ͣ���ɫ��dz
��Ϊ2NO+O2=2NO2��2NO2�����أ�?N2O4����ɫ��������Ӧ�Ƿ��ȷ�Ӧ��U�ܵײ����¶Ƚ��ͣ�����ƽ�������ƶ���NO2Ũ�Ƚ��ͣ���ɫ��dz
��
��2����ͬѧ����ͼ2��ʾװ�úϳ�SO
3��B����ˮ��ȴ��U���еĹ�����֣�C����ʢ��K
2Cr
2O
7��Һ������C�з�����������ԭ��Ӧ�����ӷ���ʽ��
Cr2O72-+3SO2+2H+=2Cr3++3SO42-+H2O
Cr2O72-+3SO2+2H+=2Cr3++3SO42-+H2O
����������Cr��Cr
3+��ʽ���ڣ��������Ƶô��������SO
3����C��ʢ��NaOH��Һ�����װ���д������Բ��㣬Ӧ��θĽ�
��e��m����������B��C֮���Cװ�û���f
��e��m����������B��C֮���Cװ�û���f
�������������ʵ��װ����ѡ����ĸ��Ų�����滻�����ü�Ҫ����˵����
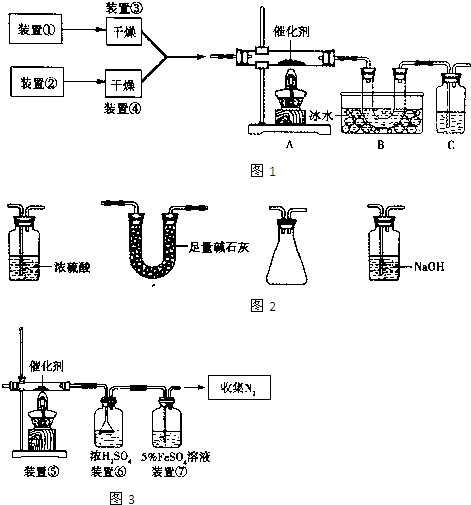
��3����ͬѧ����ͼ3��ʾװ������֤NO�ܱ�������ԭ��������ת���ʣ�װ�â١�װ�âڷֱ���NO��NH
3����������װ��A��B��C�ֱ����Тݡ��ޡ��ߣ�
��ش�װ�âߵ����ÿ�����
����δ��Ӧ��NO
����δ��Ӧ��NO
��������װ�âݵ�NO��2688mL��������Ϊ��״������ͬ������������������ռ�����״����2016ml N
2����NO��ת������
������ȷ�����������̼��ɣ�

 ��ͼ����֤ij���廯ѧ���ʵ�ʵ��װ�ã����B����A��ͨ�����������C�и���ĺ�ɫ�����ޱ仯����ر�B��C�и���ĺ�ɫ������ɫ����
��ͼ����֤ij���廯ѧ���ʵ�ʵ��װ�ã����B����A��ͨ�����������C�и���ĺ�ɫ�����ޱ仯����ر�B��C�и���ĺ�ɫ������ɫ����

 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д� ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д�
 ��2011?��ɽģ�⣩��ͼ�Ǹ��ֲ�ͬ�ܶȵ�����������Ӧ����ͬ�¶ȣ�ʱ��Ҫ��ԭ����ķֲ�ͼ���������ͼ�������ش��й����⣮
��2011?��ɽģ�⣩��ͼ�Ǹ��ֲ�ͬ�ܶȵ�����������Ӧ����ͬ�¶ȣ�ʱ��Ҫ��ԭ����ķֲ�ͼ���������ͼ�������ش��й����⣮