
【题目】三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点:33℃,沸点:73℃。实验室可用如图装置制取ICl3。
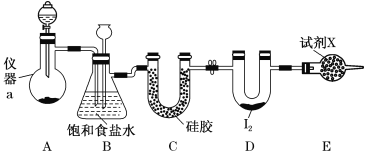
(1)仪器a的名称是________。
(2)制备氯气选用的药品为漂白精固体[主要成分为Ca(ClO)2]和浓盐酸,相关反应的化学方程式为__________________________________。
(3)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时装置B中的现象:____________________________________________。
(4)试剂X为________________。
(5)氯气与单质碘需在温度稍低于70℃下反应,则装置D适宜的加热方式为________________。
(6)500 mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管,170℃下充分反应,用水-乙醇混合液充分溶解产物I2,定容到100 mL。取25.00 mL用0.0100 mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00 mL,则样品中CO的体积分数为________。(保留三位有效数字)(已知:气体样品中其他成分与I2O5不反应;2Na2S2O3+I2===2NaI+Na2S4O6)
【答案】 蒸馏烧瓶 Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O 吸滤瓶中液面下降,长颈漏斗中液面上升 碱石灰 水浴加热 8.96%
【解析】实验室可用如图装置制取ICl3:装置A是Ca(ClO)2)和浓盐酸反应制取氯气,盐酸易挥发,反应制取的氯气中含有氯化氢、水蒸气等杂质,通过装置B中长导管内液面上升或下降调节装置内压强,B为安全瓶,可以防止倒吸,根据B中内外液面高低变化,可以判断是否发生堵塞,同时利用饱和食盐水除去氯气中的氯化氢,装置C是利用硅胶吸收水蒸气,装置D碘和氯气反应生成ICl3,氯气有毒需进行尾气处理,E装置吸收多余的氯气,防止污染空气.
(1)根据装置图可知仪器a的名称;
(2)次氯酸钙具有强的氧化性,能够氧化盐酸,生成氯化钙、氯气和水,依据化合价升级数目相同配平方程式;
(3)装置B作安全瓶,监测实验进行时C中是否发生堵塞,C发生堵塞时,B中压强增大,吸滤瓶中液面下降,长颈漏斗中液面上升;
(4)氯气有毒需进行尾气处理,可以用碱石灰吸收;
(5)水浴的温度不超过100℃,水浴能简便控制加热的温度,且能使受热容器受热均匀;
(6) 根据方程式:5CO+I2O5![]() 5CO2+I2和2Na2S2O3+I2=2NaI+Na2S4O6列关系式得:5CO~I2~2Na2S2O3;然后计算即可。
5CO2+I2和2Na2S2O3+I2=2NaI+Na2S4O6列关系式得:5CO~I2~2Na2S2O3;然后计算即可。
(1)根据装置图可知仪器a的名称为蒸馏烧瓶,
故答案为:蒸馏烧瓶;
(2)漂白粉固体和浓盐酸反应生成氯化钙、氯气和水,化学方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;
故答案为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;
(3)装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的压强增大,吸滤瓶中液面下降,长颈漏斗中液面上升,
故答案为:吸滤瓶中液面下降,长颈漏斗中液面上升;
(4)反应后剩余的氯气能够污染空气,不能排放到空气中,装置E为球形干燥管,装有固体药品碱石灰,吸收多余的氯气,防止污染空气,所以试剂X为碱石灰,
故答案为:碱石灰;
(5)因水浴能简便控制加热的温度,且能使受热反应试管受热均匀,由于氯气与单质碘需在温度稍低于70℃下反应,应采取水浴加热,
故答案为:水浴加热.
(6)由信息可知5CO+I2O5![]() 5CO2+I2,所以5CO~I2~2Na2S2O3即5CO~2Na2S2O3,n(CO)=
5CO2+I2,所以5CO~I2~2Na2S2O3即5CO~2Na2S2O3,n(CO)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ×4×(0.010 0 mol·L-1×0.02 L)=2×10-3mol,V(CO)=2×10-3mol×22.4 L·mol-1×1 000 mL·L-1=44.8 mL。
×4×(0.010 0 mol·L-1×0.02 L)=2×10-3mol,V(CO)=2×10-3mol×22.4 L·mol-1×1 000 mL·L-1=44.8 mL。
故样品中CO的体积分数=![]() ×100%=8.96%。
×100%=8.96%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】




图A 图B 图C 图D
A. 除去CO中的CO2
B. 苯萃取碘水中的I2分出水层后的操作
C. 配制0.10 mol·L-1NaOH溶液
D. 记录滴定终点读数为12.20mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学家中,提出“单质的性质,以及各元素的化合物的形态和性质,与元素的原子量数值呈周期性的变化”的是
A.道尔顿B.德谟克利特C.拉瓦锡D.门捷列夫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积相同的甲、乙两个容器中,分别充有2 mol SO2和1mol O2,在相同的温度下发生反应2SO2+O2![]() 2SO3,并达到平衡,在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
2SO3,并达到平衡,在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
A. 等于p%B. 大于p%C. 小于p%D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的分类或变化正确的是( )
①混合物:氯水、氨水、水玻璃、水银、食醋、淀粉 ②含有氧元素的化合物叫氧化物 ③CO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2 为碱性氧化物 ④同素异形体:C60、C70、金刚石、石墨 ⑤在熔融状态下能导电的化合物为离子化合物 ⑥强电解质溶液的导电能力一定强 ⑦有单质参加的反应或有单质产生的反应是氧化还原反应 ⑧煤的气化、液化、干馏都是化学变化
A. ④⑤⑧ B. ②③⑤ C. ①④⑥⑦ D. ③④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中不正确的是( )
A.工业上用CO还原赤铁矿(含Fe2O3)获得铁
B.从海产品(如海带等)中提取碘是工业上获取碘的重要途径
C.工业上可通过铝土矿获得铝
D.玛瑙、水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是白色粉末,微溶于水,酸性条件下不稳定,易生成金属 Cu 和Cu2+,广泛应用于化工和印染等行业。某研究性学习小组拟热分解 CuC122H2O 制备 CuCl,并进行相关探究。下列说法正确的是( )

A. 途径 1 中产生的Cl2 可以回收循环利用,也可以通入饱和CaCl2 溶液中除去
B. 途径 2 中 200℃时反应的化学方程式为:Cu2(OH)2Cl2![]() 2CuO+2HCl↑
2CuO+2HCl↑
C. X 气体可以是N2,目的是做保护气,抑制 CuCl22H2O 加热过程可能的水解
D. CuCl 与稀硫酸反应的离子方程式为:2CuCl+4H++SO42—=2Cu2++2Cl—+SO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线①代表滴定盐酸的曲线
B. a点溶液中: c(OH-)+c(CH3COO-)-c(H+) =0.1 mol/L
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com