
【题目】据下表中烃的分子式排列,判断空格中烃的同分异构体数目是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A.3 B.4 C.5 D.6
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是

A. 选择合适的试剂,用图甲可分别制取少量CO2、NO和O2
B. 洗涤沉淀时(见图乙),向漏斗中加入适量水,搅拌并滤干
C. 用图丙所示装置除去HCl中的少量CO2
D. 用图丁装置从KI和I2的固体混合物中回收I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积、浓度均为0.2 mol·L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示。下列说法不正确的是( )
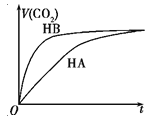
A.酸性:HB>HA>H2CO3
B.反应结束后所得两溶液中:c(A-)>c(B-)
C.上述三种溶液中由水电离的c(OH-)相对大小:NaHCO3>HA>HB
D.HA溶液和NaHCO3溶液反应所得的溶液中: c(A-)+ c(HA)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(共10分)某溶液可能含有Na+、K+、Mg2+、Cu2+等阳离子及MnO4-、SiO32-、AlO2-、CO32-、HCO3-、SO42-、Cl-等阴离子,已知:①该溶液呈无色;②经测定溶液的pH=12;③取少量溶液,加入100 mL 2 mol·L-1稀盐酸进行酸化,有白色沉淀生成,还得到一种无色无味的气体,该气体使澄清石灰水(足量)变浑浊。对酸化后的溶液过滤,得到滤液甲。
(1)由①②③可判断:原溶液中一定不存在的离子是________,一定存在的离子是 。
(2)将滤液甲分成两等份,一份中逐滴加入氨水,刚开始加入氨水时,没有沉淀产生,最终有白色胶状沉淀,说明原溶液中一定有 (填离子符号);另一份中加入足量的Ba(NO3)2溶液,有白色沉淀生成,说明原溶液中一定有 (填离子符号),过滤得到滤液乙。
(3)往滤液乙中加入足量的AgNO3溶液,过滤、洗涤、干燥得固体26.5 g,则原溶液中是否有Cl-? (填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是a、b两种固体物质的溶解度曲线。下列说法中正确的是
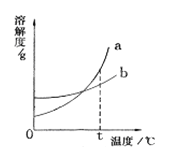
A. a物质的溶解度受温度变化的影响较小,b物质的溶解度受温度变化的影响较大。
B. t℃时,等质量的a、b饱和溶液中含有相同质量的溶质
C. 当温度大于t℃时,a溶液一定比b溶液浓
D. a中含有少量b时,用冷却热饱和溶液的方法提纯a。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是( )
A.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1
B.X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,升高温度,该反应的ΔH增大
Z(g)+W(s) ΔH>0,升高温度,该反应的ΔH增大
C.已知:S(s)+O2(g)=SO2(g) ΔH1,S(g)+O2(g)=SO2(g) ΔH2 则 ΔH1>ΔH2
D.甲中加入1 g SO2、1 g O2,乙中加入2 g SO2、2 g O2,在恒温恒容或恒温恒压下反应2SO2(g)+O2(g)![]() 2SO3(g)达平衡时,乙放出的热量都等于甲的2倍
2SO3(g)达平衡时,乙放出的热量都等于甲的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】定量的稀硫酸与过量锌粉反应,为了减慢反应速率但又不影响生成氢气总量的措施是( )
A.加入少量NaOH溶液
B.加入少量的NaHSO4溶液
C.加入少量的CH3COONa溶液
D.加入少量的CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化工生产原理错误的是( )
①可以用电解熔融氯化钠的方法来制取金属钠②可以用钠加入氯化镁饱和溶液中制取镁③用电冶铝时,原料是氯化铝④湿法炼铜是用锌和硫酸铜溶液反应置换出铜
A.②③ B.①③ C.①②③ D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com