
| A、食物溶于水后的溶液中pH<7,则为酸性食物 |
| B、由C、N、S、P等元素组成的蛋白质是酸性食物 |
| C、蔬菜、水果多含钾、钠、钙、镁等盐类及果酸,习惯称为酸性食物 |
| D、柠檬酸是酸性食物 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
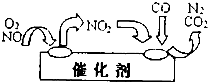 直接排放含二氧化硫、氮氧化物均会危害环境,必须对它们进行处理.
直接排放含二氧化硫、氮氧化物均会危害环境,必须对它们进行处理.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、油脂 | B、葡萄糖 |
| C、蛋白质 | D、氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
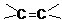 的方法是
的方法是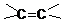 应先检验哪一个官能团?
应先检验哪一个官能团?查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能够使品红试液褪色的气体一定是SO2 |
| B、常温下,铁、铝不与浓硫酸反应,因此可以用铁、铝容器贮存运输浓硫酸 |
| C、铵盐都含有铵根离子,因此铵盐都可以与碱反应 |
| D、一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入稀氨水,平衡逆向移动,KW减小 |
| B、向水中加入少量固体硫酸钠,平衡不移动,KW不变 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、向水中加入少量固体NH4Cl,平衡正向移动,c(H+)降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com