
| A、正反应速率加快 |
| B、逆反应速率加快 |
| C、正、逆反应速率都加快 |
| D、正反应速率减慢,逆反应速率加快 |
科目:高中化学 来源: 题型:
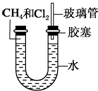 如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.
如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉和纤维素的化学式都是(C6H10O5)n,但由于n不同,淀粉和纤维素并不互为同分异构体 |
| B、鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可用灼烧的方法 |
| C、乙醇可以被酸性高锰酸钾溶液或酸性重铬酸钾溶液直接氧化成乙酸 |
| D、醇CH3CHOHCH3不能在铜或银作催化剂的条件下发生催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、该反应是焓变为负值 | |||
| B、其它条件不变,缩小容器体积,H2浓度一定增大 | |||
| C、升高温度,正反应速率增大,逆反应速率减小 | |||
D、该反应化学方程式为CO+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池跟电解池连接后,电子从电池负极流向电解池阳极 |
| B、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| C、无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液中的有效成分 |
| D、工业上铜的电解精炼时电解池中每转移1mol电子时阴极析出的铜小于0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 |
| B、需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 |
| C、吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量多 |
| D、因为3O2═2O3是吸热反应,所以臭氧比氧气的化学性质更活泼 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com