
| A、+3 | B、+2 | C、+1 | D、0 |


科目:高中化学 来源: 题型:
| A、新制的氯水在光照下颜色变浅 |
| B、Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| C、H2、I2、HI平衡混合气加压后颜色变深 |
| D、在合成氨的反应中,加压有利于氨的合成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
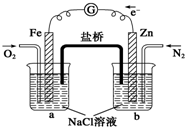
| A、烧杯a中的溶液pH不变 |
| B、烧杯a中发生氧化反应 |
| C、烧杯b中发生的反应为Zn-2e-=Zn2+ |
| D、烧杯a中发生的反应为2H2O+2e-=H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、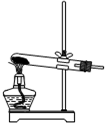 在如图所示装置中制氨气 |
| B、利用铝热反应焊接铁轨 |
| C、通过合成氨实现人工固氮 |
| D、过氧化钠用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原剂是HCl,氧化剂是MnO2 |
| B、每生成1 molCl2,转移电子的物质的量为2 mol |
| C、每消耗1 molMnO2,起还原剂作用的HCl消耗4mol |
| D、生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、溶液中c(Na+)=2c(SO42-) | ||
B、沉淀的物质的量等于
| ||
| C、标况下,生成SO2的体积<11.2aL | ||
D、原浓硫酸中H2SO4的物质的量>
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
| B、碳酸铵分解是因为外界给予了能量 |
| C、该反应的△H-T△S>0 |
| D、碳酸盐都不稳定,都能自发分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com