
Ⅰ、向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol·L -1HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。(已知:Cu2O+2H+=Cu+Cu2++H2O)
(1)Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 。
Ⅱ、一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g)  2SO3(g)。当反应达到平衡时,容器内压强变为起始时的0.7倍。
2SO3(g)。当反应达到平衡时,容器内压强变为起始时的0.7倍。
请回答下列问题:
(4)判断该反应达到化学平衡状态的标志是 (填字母)。
A.SO2、O2、SO3三者的浓度之比为2∶1∶2 B.容器内气体的压强不变
C.容器内混合气体的密度保持不变 D.SO3的物质的量不再变化
E.SO2的生成速率和SO3的生成速率相等
(5) SO2的转化率 。
(1)3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O (2分)(2)16 (2分)
(3)0.1mol(2分)(4)B、D、E;(5)90% (2分)。
【解析】
试题分析:(1)硝酸有强氧化性,Cu2O有还原性,二者会发生氧化还原反应,Cu2O跟稀硝酸反应的离子方程式是3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O;(2)根据N元素守恒可知n(N)=2n(Cu)+n(NO).所以n(Cu)= [n(N)-n(NO)]÷2=[1 L× 0.6 mol/L-0.1mol]÷2=0.25mol,因此若将上述混合物用足量的H2加热还原,所得到固体Cu的物质的量是0.25mol,其质量为0.25mol×64g/mol=16g;(3)若混合物中含0.1 mol Cu,由于混合物中含有Cu元素的物质的量为0.25mol,假设含有CuO的物质的量为x,则含有Cu2O的物质的量为(0.25-0.1-x)/2mol,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为根据电子转移守恒,混合物中n(Cu2O)=(0.1×3-0.1×2)mol÷2=0.05mol;再结合(2)中Cu元素物质的量计算混合物中n(CuO)=(0.25-0.1-0.05×2)mol=0.05mol,根据Cu不与稀H2SO4反应,Cu2O、CuO与稀H2SO4反应,Cu2O、CuO与硫酸发生反应时物质的量的比为1:1可知 0.05molCu2O、0.05molCuO共消耗硫酸的物质的量为n(H2SO4)=0.05mol+0.05mol=0.1mol。(4) A.物质反应时是按照2∶1∶2关系进行的,但是反应达到平衡时的物质的量浓度关系可能是该比例,也可能不是,因此不能作为判断平衡的标志,错误;B.由于该反应是反应前后气体体积不等的反应,所以若反应未达到平衡,则容器内的压强就会发生变化,所以容器内气体的压强不变可以作为反应达到平衡的标志,正确;C.化学反应遵循质量守恒定律,所以在任何时刻反应容器内混合气体的密度都保持不变,故不能作为判断平衡的标志,错误;D.若SO3的物质的量不再变化,则物质的浓度就不变,反应达到平衡,正确;E.由于每产生1个SO2就会同时消耗1个SO3,若SO2的生成速率和SO3的生成速率相等,则SO2和SO3的浓度保持不变,反应达到平衡,因此可以作为判断化学反应平衡的标志,正确。(5) 在恒容的密闭容器内气体压强是原来的0.7倍,则气体的物质的量的开始时的0.7倍。假设反应消耗O2的物质的量为x,则消耗SO2的物质的量为2x;达到平衡时各种气体的物质的量为SO2: (0.4 -2x)mol ;O2:(0.2 -x)mol;SO3: 2xmol;根据题意可得{(0.4 -2x)+(0.2 -x)+ 2x )÷(0.4+0.2)=0.7,解得x=0.18mol,所以发生反应的SO3的物质的量为0.36mol,故SO2的转化率(0.36mol÷0.4mol)×100%=90%。
考点:考查氧化还原反应的离子方程式的书写、守恒法在化学计算中的应用、可逆反应平衡状态的判断、物质转化率的计算的知识。


 综合自测系列答案
综合自测系列答案科目:高中化学 来源:2015届浙江省高二下学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.糖类、油脂、蛋白质都是高分子化合物,它们水解的最终产物不相同
B.检验溴乙烷中的溴元素,可以在溴乙烷中加入AgNO3溶液
C.葡萄糖在一定条件下能水解生产乙醇与二氧化碳
D.苯酚能与溴水反应,苯不能与溴水反应,说明羟基对苯环有影响
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:推断题
黄酮醋酸(F)具有独特抗癌活性,它的合成路线如下:

已知:RCN在酸性条件下发生水解反应: RCN 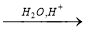 RCOOH
RCOOH
(1)上述路线中A转化为B的反应为取代反应,写出该反应的化学方程式
_________________________________________________________________。
(2)F分子中有3种含氧官能团,名称分别为醚键、_____________和______________。
(3)E在酸性条件下水解的产物可通过缩聚反应生成高分子化合物,该高分子化合物的结构简式为_________________________。
(4)写出2种符合下列条件的D的同分异构体的结构简式_____________、________________。
①分子中有4种化学环境不同的氢原子
②可发生水解反应,且一种水解产物含有酚羟基,另一种水解产物含有醛基。
(5)对羟基苯乙酸乙酯(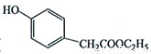 )是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。
)是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。
合成路线流程图请参考如下形式:

查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列实验可达到实验目的的是( )
A.将苯与浓硝酸、浓硫酸的混合物在60℃水浴加热条件下反应可生成硝基苯
B.用酸性高锰酸钾溶液即可检验CH2=CH-CHO中的碳碳双键
C.将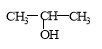 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2
D.淀粉在硫酸催化作用下水解,将银氨溶液加入到水解后的溶液中可检验淀粉水解的产物葡萄糖
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是 ( )
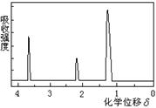
A.C2H5OH B.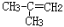 C.CH3CH2CH2COOH D.
C.CH3CH2CH2COOH D.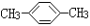
查看答案和解析>>
科目:高中化学 来源:2015届浙江省“温州八校”高三返校联考化学试卷(解析版) 题型:选择题
常温下,用 0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如下图所示,则下列说法正确的是
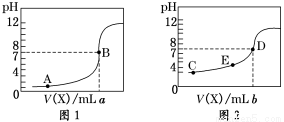
A.图2是滴定盐酸的曲线
B.a与b的关系是:a<b
C.E点对应离子浓度由大到小的顺序为: c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.这两次滴定都可以用甲基橙作为指示剂且颜色变化为红变橙
查看答案和解析>>
科目:高中化学 来源:2015届浙江省“温州八校”高三返校联考化学试卷(解析版) 题型:选择题
一定条件下,0.3 mol X(g)与0.3 mol Y(g)在体积为1L的密闭容器中发生反应:
X(g)+3Y(g) 2Z(g),下列示意图合理的是
2Z(g),下列示意图合理的是

查看答案和解析>>
科目:高中化学 来源:2015届河南长葛第三实验高中高二下学期第一次考试化学试卷(解析版) 题型:计算题
某烃类物质0.1mol完全燃烧,将生成物通过浓硫酸,浓硫酸增重7.2克,再将剩余气体通过碱石灰,碱石灰增重13.2克,通过计算,
(1)确定该有机物的最简式
(2)确定该有机物的分子式,写出其结构简式。
(3)该烃标态下对氢气的相对密度为多少
查看答案和解析>>
科目:高中化学 来源:2015届河南省顶级名校高三入学定位考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.铝制容器可盛 装热的浓H2SO4 B.AgI胶体在电场中自由运动
C.K与水反应比Li与水反应剧烈 D.红磷在过量Cl2中燃烧生成PCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com