
【题目】下列根据实验操作和现象所得出的结论不正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 在A1C13溶液中逐滴滴入NaOH溶 液至过量,然后通入CO2气体 | 先出现白色沉淀,后沉淀消失,最后又出现白色沉淀 | Al(OH)3是两性氢氧化物,但不能溶解在某些弱酸中 |
B | 向浓度均为0.1mol/L的MgCl2、 CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
C | 向Na2CO 3溶液中加入浓盐酸,将产生的气体通入硅酸钠溶液中 | 产生白色浑浊 | 酸性:盐酸>碳酸>硅酸 |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在I3- |
A. A B. B C. C D. D
【答案】C
【解析】A. 在A1C13溶液中逐滴滴入NaOH溶液至过量,先出现白色沉淀,后沉淀消失,生成偏铝酸钠溶液,通入CO2气体,又反应生成氢氧化铝沉淀,说明Al(OH)3是两性氢氧化物,但不能溶解在某些弱酸中,故A正确;B.溶度积小的先生成沉淀,向浓度为0.1molL-1的MgCl2、CuCl2混合溶液中逐滴加入氨水先出现蓝色沉淀,说明Ksp[Cu(OH)2]较小,故B正确;C.盐酸易挥发,盐酸与硅酸钠反应也能生成硅酸沉淀,则该实验不能比较碳酸和硅酸的酸性强弱,故C错误;D.溶液变蓝色,说明含有碘单质,有黄色沉淀,说明含有碘离子,则溶液中存在平衡:I3-I2+I-,故D正确;故选C。


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】燃烧1g乙炔生成二氧化碳和液态水,放出热量50kJ,则这一反应的热化学反应方程式为( )
A.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+50 kJ?mol﹣1
B.C2H2(g)+ ![]() O2(g)═2CO2(g)+H2O(g)△H=﹣1300 kJ?mol﹣1
O2(g)═2CO2(g)+H2O(g)△H=﹣1300 kJ?mol﹣1
C.2C2H2+5O2═4CO2+2H2O△H=﹣2 600 kJ
D.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2600 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在强碱性溶液中可以大量共存的是( )
A. K+、Na+、H+、Cl- B. Na+、Ba2+、NO3-、Cl-
C. K+、NH4+、S2-、CO32- D. Ca2+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,有下列分子数相同的可逆反应,其平衡常数K值分别是 ①H2+F22HF K=1047
②H2+Cl22HCl K=1017
③H2+Br22HBr K=109
④H2+I22HI K=1
比较K值大小,可知各反应的正反应进行的程度由大到小的顺序是( )
A.①②③④
B.④②③①
C.①④③②
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.做焰色反应前铂丝要先在硫酸中洗涤,再在酒精灯上灼烧至无色
B.AgBr是一种重要的感光材料,可用于制作照相底片
C.新制的氯水应保存在无色广口瓶中,并放在阴凉处
D.碘是人体必需的微量元素,所以人每天要要适当补充含I2的食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 向氯化亚铁溶液中通入氯气:Fe2++Cl2 === Fe3++2Cl-
B. 将氯气通入冷的氢氧化钠溶液中:Cl2+2OH- === Cl- + ClO- + H2O
C. 氯化铝溶液与过量氢氧化钠溶液反应:Al3+ + 3OH- === Al(OH)3↓
D. 金属铝加热条件下溶于硝酸:2Al+6H+ === 2Al3+ + 3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料,二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g) ![]() N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/(mol/L)/\时间/min | 0 | 10 | 20 | 30 | 40 |
NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 |
N2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
①若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:3:3,则达到新平衡时NO的转化率______________(填“升高”或“降低”),△H_____0(填“>”或“<”)。
②根据图表数据分析T1℃时,该反应在0~10min内的平均反应速率v(N2)=______________mol·L-1·min-1;计算该反应的平衡常数K=_____________。
③若30min后只改变某一条件,据上表中的数据判断改变的条件可能是____________(填字母编号)。
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式_______________________。
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:_______________________。
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10 的溶液,则溶液中c(CO32-)∶c(HCO3-)=_______________。[常温下K1(H2CO3)=4.4×10-7、 K2(H2CO3)=5×10-11]。
②欲用2LNa2CO3溶液将4.66gBaSO4 固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为__________________________。[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10]。(忽略溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,用如图所示装置(尾气处理装置略去)进行下列实验,将①中液体逐滴滴入到②中。预测的现象与实际不相符的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质。下列判断正确的是
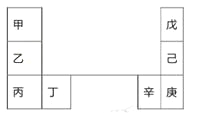
A. 金属性:甲>乙>丁
B. 原子半径:辛>己>戊
C. 丙和庚的原子核外电子数相差11
D. 乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com