
【题目】
①过滤 ②蒸发 ③向容量瓶转移液体
A. ①和③ B. ①和② C. ②和③ D. ①②③
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】全世界每年被腐蚀损耗的钢铁材料约占全年钢铁产量的十分之一。研究钢铁的腐蚀及防护有重要意义。回答下列问题:
(1)钢铁发生腐蚀的主要类型是电化学腐蚀,在电化学腐蚀中,负极反应是_____________,正极反应是_____________。
(2)某实验小组设计下列实验探究铁生锈的条件:
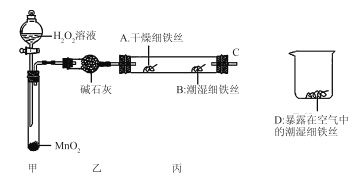
反应4 min后观察,发现A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮。该实验说明铁生锈主要与_________和___________有关;B、D处实验现象对比说明:决定铁生锈的一个重要因素是___________。
(3)金属及塑料制品表面镀铬不仅美观还可提高金属制品抗腐蚀性能。常见镀铬液由重铬酸(H2Cr2O7)和催化剂硫酸组成。
①重铬酸中,Cr元素的化合价为________。
②镀铬时由CrO42-放电产生铬镀层。阴极的电极反应式为_______。
(4)电镀废水中Cr2O72-具有高毒性,必须经处理后才能排放。电解法处理含铬的强酸性废水的原理如右图所示。
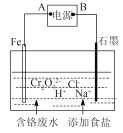
电解产生的Fe2+将Cr2O72-还原为Cr3+,再随着溶液pH的升高,便有Fe(OH)3和Cr(OH)3沉淀生成。
①图中A为电源__________极;电解时阴极产生的气体为____________(写化学式)。
②写出Fe2+与Cr2O72-反应的离子方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
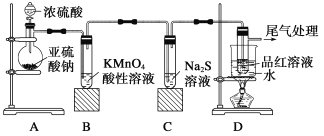
请回答:
(1)装置A中蒸馏烧瓶生成SO2的化学方程式为: 。
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为: 。
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象: 。
Ⅱ.某化学兴趣小组为探究铜跟浓硫酸的反应,用图所示装置进行有关实验。请回答:
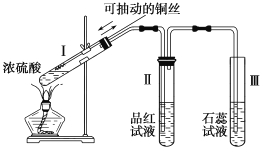
(4)试管Ⅰ中发生反应的化学方程式为:: 。
(5)下列实验不合理的是 。
A.上下移动Ⅰ中铜丝可控制生成SO2的量
B.Ⅱ中选用品红溶液验证SO2的生成
C.Ⅲ中可选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向Ⅰ加水,观察溶液颜色
(6)实验中,用ag铜片和VmL18.4mol·L-1的浓硫酸(98%)放在试管中共热,直到反应完毕,发现试管中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余。
①有一定量的硫酸剩余但未能使铜片完全溶解,你认为原因是 。
②下列药品中能用来证明反应结束后的试管中确有硫酸剩余的是 (填序号)。
a.铁粉 b.BaCl2溶液 c.Ba(NO3)2溶液 d.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图a、b、c、d均为铂电极,供选择的电解质溶液如下表( )
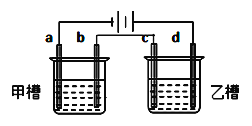
要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;
②b、c两极放电离子的物质的量相等。则应选用的电解液是
组 | A | B | C | D |
甲槽 | NaOH | Cu(NO3)2 | KCl | Na2SO4 |
乙槽 | CuSO4 | NaCl | AgNO3 | NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,不正确的是
A.用NaOH溶液除去铝箔表面的氧化膜,Al2O3 + 2OH-=2AlO2-+ H2O
B.向AlCl3溶液中加入过量氨水,Al3+ + 3NH3·H2O=Al(OH)3↓ + 3NH4+
C.用胃舒平(复方氢氧化铝)缓解胃酸(HCl)过多,OH-+ H+=H2O
D.向污水中投放明矾,生成能凝聚悬浮物的胶体,Al3+ + 3H2O![]() Al(OH)3 (胶体) + 3H+
Al(OH)3 (胶体) + 3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
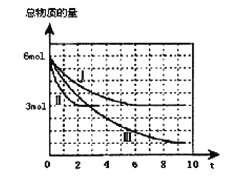
【题目】甲醇是一种可再生的清洁能源,一定条件下用CO和H2合成CH3OH:CO(g)+2H2 (g)![]() CH3OH(g)H =a kJ·mol-1。向体积为2 L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内气体总物质的量随时间(min)的变化关系如下左图中Ⅰ、Ⅱ、Ⅲ曲线所示:
CH3OH(g)H =a kJ·mol-1。向体积为2 L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内气体总物质的量随时间(min)的变化关系如下左图中Ⅰ、Ⅱ、Ⅲ曲线所示:
(1)能判断反应达到化学平衡状态的是 (填字母)。
A.c(CO)与c(H2)的比值保持不变
B.容器中气体压强保持不变
C.容器中气体密度保持不变
D.单位时间内有1molCO消耗的同时有1mol CH3OH生成
E.v正(H2)=2 v逆(CH3OH)
(2)①Ⅱ和Ⅰ相比,Ⅱ改变的反应条件是 。
②反应Ⅲ在9min时达到平衡,比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1 T3(填“>”“<”“=”),此正反应是________反应(填“放热或吸热”)。
(3)①反应Ⅰ在6 min时达到平衡,从反应开始到达到平衡时v (CH3OH) = mol/(L·min)。
②反应Ⅱ在2 min时达到平衡,计算该温度下的平衡常数K= 。在体积和温度不变的条件下,在上述反应达到平衡Ⅱ时,再往容器中加入1 mol CO和3 mol CH3OH后,平衡将向_________(填“正反应、逆反应和不移动”),原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某非金属单质A和氧气发生化合反应生成B,B为气体,其体积是反应掉氧气体积的两倍(同温同压)。关于B分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子 C.有1个A原子 D.有2个A原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com