
����Ŀ���״���һ�ֿ������������Դ,һ����������CO��H2�ϳ�CH3OH:CO��g��+2H2 ��g��![]() CH3OH��g��H =a kJ��mol-1�������Ϊ2 L���ܱ������г���2mol CO��4mol H2����ò�ͬ�¶������������������ʵ�����ʱ����min���ı仯��ϵ������ͼ��������������ʾ��
CH3OH��g��H =a kJ��mol-1�������Ϊ2 L���ܱ������г���2mol CO��4mol H2����ò�ͬ�¶������������������ʵ�����ʱ����min���ı仯��ϵ������ͼ��������������ʾ��
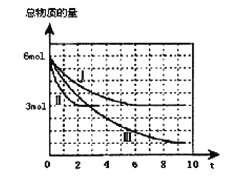
��1�����жϷ�Ӧ�ﵽ��ѧƽ��״̬���� ������ĸ����
A��c��CO����c��H2���ı�ֵ���ֲ���
B������������ѹǿ���ֲ���
C�������������ܶȱ��ֲ���
D����λʱ������1molCO���ĵ�ͬʱ��1mol CH3OH����
E��v����H2����2 v����CH3OH��
��2���٢������ȣ���ı�ķ�Ӧ������ ��
�ڷ�Ӧ����9minʱ�ﵽƽ�⣬�ȽϷ�Ӧ����¶���T1���ͷ�Ӧ����¶���T3���ĸߵͣ�T1 T3���>����<����=������������Ӧ��________��Ӧ������Ȼ����ȡ�����
��3���ٷ�Ӧ����6 minʱ�ﵽƽ�⣬�ӷ�Ӧ��ʼ���ﵽƽ��ʱv ��CH3OH�� = mol/��L��min����
�ڷ�Ӧ����2 minʱ�ﵽƽ�⣬������¶��µ�ƽ�ⳣ��K= ����������¶Ȳ���������£���������Ӧ�ﵽƽ���ʱ�����������м���1 mol CO��3 mol CH3OH����ƽ�⽫��_________�������Ӧ���淴Ӧ�Ͳ��ƶ�������ԭ����______________��
���𰸡���1��BE
��2����ʹ�ô�������>������
��3����1/8����0.125mol/��L.min����
��12�����ƶ�����Ϊƽ������������1molCO��3molCH3OH��
��ʱ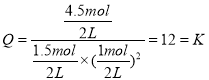 ������ƽ�ⲻ�ƶ�
������ƽ�ⲻ�ƶ�
��������
�����������1��Ͷ�ϱȵ���ϵ���ȣ�c��CO����c��H2���ı�ֵ�Ƕ�ֵ��c��CO����c��H2���ı�ֵ���ֲ��䲻һ��ƽ�⣻��Ӧǰ������ϵ���Ͳ�ͬ��ѹǿ�DZ���������������ѹǿ���ֲ���һ��ƽ�⣻��λʱ������1molCO���ĵ�ͬʱ��1mol CH3OH���ɣ���������Ӧ���ʣ����Բ�һ��ƽ�⣻���淴Ӧ���ʱȵ���ϵ���ȣ�v����H2����2 v����CH3OH��һ��ƽ�⣻��2���٢������ȣ���Ӧ���ʼӿ죬ƽ�ⲻ�ƶ�����ı�ķ�Ӧ�����Ǽ������������Ӧ�������������Ӧ����¶ȵͣ�T1 >T3�������¶�ƽ�������ƶ�������Ӧ���ȣ���3�� �ٸ������⣬�����ɼ״������ʵ���Ϊxmol

2-x+4-2x+x=3���X=1.5mol
v ��CH3OH��=1.5mol��2 L��6 min=0.125 mol/��L.min����
��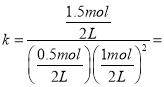 12��
12��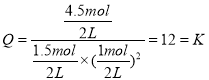 ����ƽ�ⲻ�ƶ���
����ƽ�ⲻ�ƶ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ư����Һ���ݹ�����ɫ��������������ڿ����У�����һ��ʱ�䣬��Ư��Ч������õ�ԭ�������
A. Ư�۱�������
B. ��ɫ�����������е�����������
C. Ư����Һ�������е�CO2�ķ�Ӧ��֣������˽϶����Ĵ�����
D. Ư����Һ����������ˮ����Ũ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����MnO2Ϊԭ���Ƶõ�MnCl2��Һ�г�����Cu2+��Pb2+�Ƚ������ӣ�ͨ�����ӹ������ܵ����MnS����ʹ��Щ���������γ���������������˳�ȥ����MnS���ڵij�������������ʵ����ʵ������˵���У�����ȷ����
A���ܽ�� MnS��PbS
B��MnS���ڳ����ܽ�ƽ�� MnS(s)![]() Mn2+(aq) + S2-(aq)
Mn2+(aq) + S2-(aq)
C��Cu2+ת��Ϊ������ԭ��Ϊ MnS(s) + Cu2+(aq)=CuS(s) + Mn2+(aq)
D������ת�������ڳ�ȥ��Һ�е�ijЩ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Q��Ԫ�����ڱ��е����λ����ͼ��ʾ������˵����ȷ���ǣ� ��

A. Ԫ��X��Ԫ��Z����������ϼ�֮�͵���ֵ����8
B. ԭ�Ӱ뾶�Ĵ�С˳��Ϊ��rX��rY��rZ��rW��rQ
C. ����Y2����Z3+�ĺ���������͵��Ӳ���������ͬ
D. Ԫ��W������������Ӧ��ˮ��������Ա�Q��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
������ ������ ��������ƿת��Һ��
A. ������ B. ������ C. ������ D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijУ��ѧ��ȤС��ͬѧ����ʵ���õ�����������ͬ����������SO2������
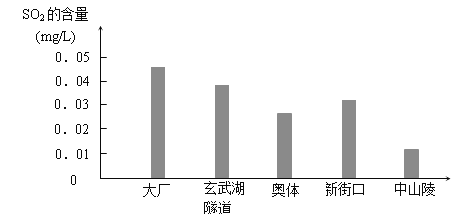
�������������SO2�������Ը�������������ԭ���� ��
���������������г��ֱ����һ����������������SO2�����Ľ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������һ���ܴ���������ǣ� ��
A.����ɫ��Һ�У�NH4+��Fe2+��SO42����CO32��
B.�ں�����Ba2+����Һ�У�NH4+��Na+��Cl����OH��
C.��ǿ����Һ�У�Na+��K+��Cl����SO32��
D.��pH=1����Һ�У�K+��Fe2+��Cl����CH3COO��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����xR2++yH++O2�TmR3++nH2O�����ӷ���ʽ�У���ϵ��m��R3+���ж���ȷ���ǣ� ��
A.m=4��R3+����������
B.m=n��R3+����������
C.m=2��R3+�ǻ�ԭ����
D.m=y��R3+�ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���3 mol A��1 mol B�����������ڹ̶��ݻ�Ϊ2 L���ܱ������У��������·�Ӧ��3A��g��+B��g�� xC��g��+2D��s����2 minĩ�÷�Ӧ�ﵽƽ�⣬����0.8 mol D�������C��Ũ��Ϊ0.2 mol��L-1�������ж���ȷ���ǣ� ��
A. �ӿ�ʼ��ƽ��A��ƽ����Ӧ����Ϊ0.3 mol��L-1��s-1
B. �ӿ�ʼ��ƽ��B��ת����Ϊ60%
C. �˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK =![]()
D. �����������ܶȲ��ٸı䣬��÷�Ӧ�ﵽƽ��״̬
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com