
【题目】对废银合金触电材料进行分离回收既节约矿物资源,又可以减少环境污染。某废银合金触电材料含Ag、Cu、Sn等,现欲利用以下工艺流程回收其中的金属资源。
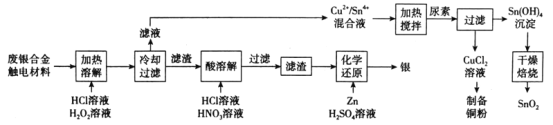
回答下列问题:
(1)“加热溶解”时Cu发生的离子方程式为_________。
(2)“加热溶解”时温度常控制在50℃左右,温度不宜过高也不宜过低的原因为_________。
(3)“酸溶解”过程中会产生少量遇空气变为红棕色的无色气体,则“酸溶解”过程主要的化学方程式为_____________。
(4)常温下,Cu2+/Sn4+混合液中c(Cu3+)=0.022mol·L-1,将混合液“加热搅拌”后冷却至室温,再加“尿素”调节溶液的pH范围为__________。(当溶液中的离子浓度小于10-5mol·L-1时,沉淀完全,已知:Ksp[Sn(OH)4]=1×10-55;Ksp[Cu(OH)2]=2.2×10-20)
(5)检验Sn(OH)4沉淀是否洗涤干净的方法是____________。
(6)用惰性电极电解CuCl2溶液,阴极反应式是___________,若想由CuCl2溶液得到无水CuCl2固体,则需进行的实验操作为_______________。
【答案】Cu+2H++H2O2![]() Cu2++2H2O 低于50℃,溶解反应较慢,超过50℃,H2O2分解与HCl逸出导致溶解翻译速率下降 3Ag+HNO3+3HCl===3AgCl↓+NO↑+2H2O 1.5≤pH<5 取最后一次洗涤液少量于试管中,滴入稀硝酸,再加入硝酸银溶液,若没有白色沉淀生成,证明洗涤干净,反之,沉淀没有洗涤干净 Cu2++2e-===Cu 将CuCl2溶液在HCl气流中加热蒸干
Cu2++2H2O 低于50℃,溶解反应较慢,超过50℃,H2O2分解与HCl逸出导致溶解翻译速率下降 3Ag+HNO3+3HCl===3AgCl↓+NO↑+2H2O 1.5≤pH<5 取最后一次洗涤液少量于试管中,滴入稀硝酸,再加入硝酸银溶液,若没有白色沉淀生成,证明洗涤干净,反之,沉淀没有洗涤干净 Cu2++2e-===Cu 将CuCl2溶液在HCl气流中加热蒸干
【解析】
结合题干信息,根据工艺流程图分析可知,某废银合金触电材料含Ag、Cu、Sn等,在加热、溶解的条件下通入H2O2和HCl溶液,Cu和Sn变成Cu2+和Sn4+,再通入尿素在加热的条件下得到CuCl2溶液和Sn(OH)4沉淀,最终经过系列操作得到铜粉和SnO2,Ag单质以滤渣的形式经过HNO3和HCl溶液的溶解得到AgCl的沉淀,再加入Zn和H2SO4溶液进行化学反应得到Ag单质,据此分析解答问题。
(1)根据上述分析,“加热溶解”时,Cu与HCl、H2O2反应变为Cu2+,离子反应方程式为Cu+2H++H2O2![]() Cu2++2H2O,故答案为:Cu+2H++H2O2
Cu2++2H2O,故答案为:Cu+2H++H2O2![]() Cu2++2H2O;
Cu2++2H2O;
(2)温度过低,反应速率慢,温度过高,反应物H2O2分解,则温度不宜过高也不宜过低的原因是低于50℃,溶解反应较慢,超过50℃,H2O2分解与HCl逸出导致溶解翻译速率下降,故答案为:低于50℃,溶解反应较慢,超过50℃,H2O2分解与HCl逸出导致溶解翻译速率下降;
(3)根据上述分析可知,“滤渣”主要成分为Ag,“酸溶解”过程为Ag和HNO3、HCl反应得到AgCl的沉淀,化学反应方程式为:3Ag+HNO3+3HCl===3AgCl↓+NO↑+2H2O,故答案为:3Ag+HNO3+3HCl===3AgCl↓+NO↑+2H2O;
(4)调节pH为保证Sn4+沉淀完全(离子浓度小于10-5mol·L-1),按c(Sn4+)=1×10-5 mol·L-1进行计算,根据Ksp[Sn(OH)4]=1×10-55可得,c(OH-)=1×10-12.5 mol·L-1,则c(H+)=1×10-1.5 mol·L-1,pH=1.5,为保证Cu2+(0.022 mol·L-1)不沉淀,按c(Cu2+)=0.022 mol·L-1进行计算,根据Ksp[Cu(OH)2]=2.2×10-20可得,c(OH-)=1×10-9 mol·L-1,则c(H+)=1×10-5 mol·L-1,pH=5,则pH的取值范围1.5≤pH<5,故答案为:1.5≤pH<5;
(5)沉淀中可能附着的有Cl-,检验是否洗净的方法可以是取最后一次洗涤液少量于试管中,滴入稀硝酸,再加入硝酸银溶液,若没有白色沉淀生成,证明洗涤干净,反之,沉淀没有洗涤干净,故答案为:取最后一次洗涤液少量于试管中,滴入稀硝酸,再加入硝酸银溶液,若没有白色沉淀生成,证明洗涤干净,反之,沉淀没有洗涤干净;
(6)惰性电极电解CuCl2溶液时,阴极Cu2+得到电子,电极反应为Cu2++2e-===Cu,由于CuCl2会水解,可在蒸发时通入HCl气体抑制水解,故答案为:Cu2++2e-===Cu;将CuCl2溶液在HCl气流中加热蒸干。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)是一种重要的半导体材料。某工厂利用铝土矿(成分为Al2O3、Ga2O3、Fe2O3等)为原料制备GaN的流程如下图所示:
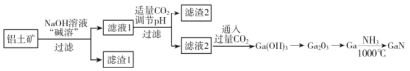
已知:镓与铝同主族,镓的熔点是29.8°C,沸点是2403°C;其氧化物和氢氧化物均为两性化合物;氢氧化物的电离常数如下:
两性氢氧化物 | Al( OH)3 | Ga( OH)3 |
酸式电离常数Ka | 2×10-11 | 1×10-7 |
碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
回答下列问题:
(1)为了提高 “碱溶”效率应采用的措施是__________(回答两种措施)。
(2)滤渣1的成分是_________。
(3)滤液2中通入过量CO2的理由是________(用离子方程式表示)。
(4)流程中利用镓与NH3在1000℃反应生成固体半导体材料 GaN,每生成l molGaN时放出15. 45 kJ热量,写出该反应的热化学方程式________。
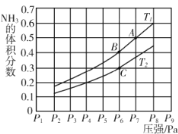
(5)在密闭容器中,充入一定量的Ga与NH3发生反应 ,测得反应平衡体系中NH3的体积分数与压强 P和温度T 的关系曲线如下图所示。图中A 点和C点化学平衡常数的大小关系: KA____KC (填“<”“=”或 “ > ”) , 判断的依据是________。
(6)已知铝土矿中Ga2O3的质量分数为 a%,某工厂使用 w 吨铝土矿经过一系列反应, 反应过程中镓元素的总利用率为 b%能制得________吨氮化镓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据vt图分析外界条件改变对可逆反应A(g)+3B(g) ![]() 2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
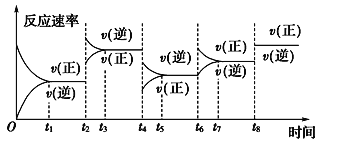
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是
A. 使用了催化剂、增大压强、减小反应物浓度、降低温度
B. 升高温度、减小压强、减小反应物浓度、使用了催化剂
C. 增大反应物浓度、使用了催化剂、减小压强、升高温度
D. 升高温度、减小压强、增大反应物浓度、使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑![]() 的水解,pAg=
的水解,pAg=![]() lgc(Ag+)),下列说法正确的是
lgc(Ag+)),下列说法正确的是
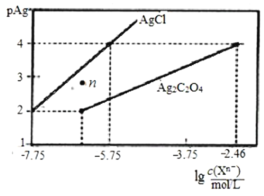
A.KspAg2C2O4的数量级等于10-10
B.n点表示AgCl的过饱和溶液
C.向c(Cl-)=c(![]() )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
D.Ag2C2O4+2Cl-![]() 2AgCl+
2AgCl+![]() 的平衡常数为103.29
的平衡常数为103.29
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
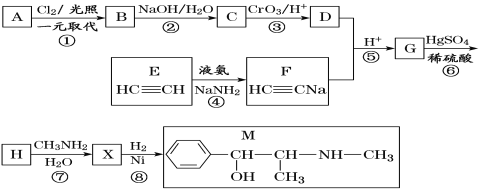
已知:I.R—CH2OH![]() RCHO
RCHO
II.R1-CHO+R-C≡CNa![]()
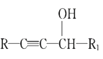
IV.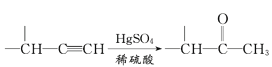
V.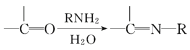
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个2L的密闭容器中,投入反应物,发生反应2SO3(g)![]() 2SO2(g)+O2(g) ΔH>0,其中SO3的变化如下图所示:
2SO2(g)+O2(g) ΔH>0,其中SO3的变化如下图所示:
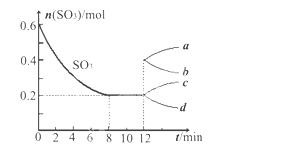
(1)写出该反应的平衡常数表达式并根据8min时到达平衡计算出结果________________。
(2)用O2表示0到8min内该反应的平均速率v=__________________。
(3)升高温度,该反应的K值将______;容器中气体的平均相对分子质量将______。(填“增大”“减小”或“不变”)
(4)能说明该反应已达到平衡状态的是________。
A.v(SO3)=2v(O2) B.容器内压强保持不变
C.v(SO2)逆=2v(O2)正 D.容器内密度保持不变
(5)在第12min时,容器压缩到1L,则SO3的变化曲线为_______。
A.a B.b C.c D.d
(6)若保持容积不变在第12min时,加入SO3(g),则平衡向_______反应方向移动(填“正” 或“逆”)。SO3的体积分数_______(填“增大”或“减小”)。
(7)将相同物质的量的SO3充入下面的两个容器中,已知甲容器有活塞可以上下移动,乙容器体积固定,在相同的温度、压强下开始发生反应,在反应过程中维持体系温度不变。
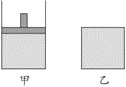
①反应达平衡所需时间甲________乙(填“大于”“等于”或“小于”);达平衡时SO3的转化率甲__________乙(“大于”“等于”或“小于”)。
②若平衡后,向甲、乙中分别充入惰性气体,__________(填“甲”或“乙”)容器的平衡将向__________(填“正”或“逆”)反应方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按照课本实验要求,用50mL0.50mol/L的盐酸于50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热,下列说法中,正确的是( )
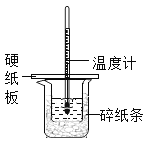
A. 烧杯间填满碎纸条的作用是固定小烧杯
B. 用如图装置可以完成中和热测定的实验
C. 为防止混合溶液时溅出产生误差,因此混合时速度要慢
D. 若将盐酸体积改为60mL,不考虑热量损失,理论上所求中和热相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC(X)=-lgc(X),pKa=-lgKa,常温下,某浓度H2A溶液在不同pH下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示,下列说法正确的是
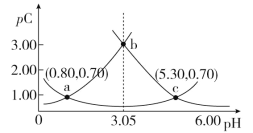
A.随着pH的增大,pC增大的曲线是A2-的物质的量浓度的负对数
B.pH=4.50时,c(HA-)>c(A2-)=c(H2A)
C.b点时, =104.50
=104.50
D.pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组用酸性KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件反应速率的影响,设计了如下探究实验方案:
实验 | 草酸溶液 (0.5mol/L) | 高锰酸钾 (0.5mol/L) | 稀硫酸 (0.5mol/L) | 硫酸锰 (0.5mol/L) | 温度 | 蒸馏水 |
① | 10.0 mL | 2.0 mL | 3.0 mL | 0 | 25℃ | 1.0 mL |
② | 10.0 mL | 2.0 mL | 3.0 mL | 1.0 mL | 25℃ | 0 |
③ | 8.0 mL | 2.0 mL | 3.0 mL | 0 | 25℃ | Vx |
④ | 10.0 mL | 2.0 mL | 3.0 mL | 0 | 35℃ | 1.0 mL |
回答下列问题:
(1)本方案中用于设计实验的化学反应的离子方程式是____,实验中预计通过观察什么现象或测定什么数据来进行判断:_____。
(2)该实验的目的是____。
(3)实验③中的Vx=____;实验①和④测得反应速率分别为v1、v4,则v1____v4(填:“>”“<”和“=”)
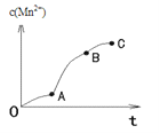
(4)实验①中,c(Mn2+)与t关系如图所示。AB段斜率明显大于OA段斜率,除反应可能放热外,猜想还可能是_____,利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1 mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
①补全实验III的操作:向试管中先加入1mL 0.01mol/L酸性KMnO4溶液,再加入10滴3mol/L硫酸,然后加入少量的____,最后加入1mL 0.1 mol/L草酸溶液。
②若猜想成立,应观察到的实验现象是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com