
【题目】水的电离平衡如图所示.

(1)若A点表示25℃时水的电离平衡状态,当升高温度至100℃时水的电离平衡状态为B点,则此时水的离子积为___________
(2)将100℃时pH=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为_________________
【答案】1×10-12 2:9
【解析】
(1)KW= c(OH-)c(H+),由图象分析可以知道c(H+)=c(OH-)=10-6mol/L,据此求出该温度下的KW;
(2)先根据水的离子积常数计算氢氧化钡溶液中c(OH-)、混合溶液中c(OH-),再根据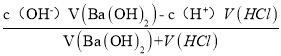 /计算氢氧化钡和盐酸的体积之比。
/计算氢氧化钡和盐酸的体积之比。
(1)25℃时纯水中c(H+)=c(OH-)=10-7 mol/L,KW= c(OH-)c(H+)=10-14,当温度升高到100℃,纯水中c(H+)=c(OH-)=10-6 mol/L, KW= c(OH-)c(H+)= 1×10-12;
因此,本题正确答案是:1×10-12;
(2)将pH=8的Ba(OH)2溶液中c(OH-)=10-4 mol/L,pH=5的稀盐酸中c(H+)=10-5mol/L,设氢氧化钡的体积为x,盐酸的体积为y,混合溶液的pH=7,溶液呈碱性, c(OH-)=![]() =10-5 mol/L,c(OH-)=(
=10-5 mol/L,c(OH-)=(![]() ) = 10-5mol/L,解之得x:y=2:9;
) = 10-5mol/L,解之得x:y=2:9;
因此,本题正确答案是:2:9。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,向某容积恒定的密闭容器中充入1 mol N2、3 mol H2,经充分反应后达到如下平衡:N2(g)+3H2(g)![]() 2NH3(g),下列有关说法中正确的是( )
2NH3(g),下列有关说法中正确的是( )
A. 达平衡后再加入一定量的N2,体系内各物质含量不变
B. N2、H2、NH3的浓度一定相等
C. 反应没有达到平衡时,NH3会不断地分解,达到平衡时则不会再分解
D. 平衡时,N2、H2物质的量之比为1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传感器可以检测空气中SO2的含量,传感器工作原理如下图所示。下列叙述正确的是( )

A.b为电源的正极
B.负极反应式 Ag - e- + Cl- = AgCl
C.当电路中电子转移为5×10-5 mol时进入传感器的SO2为 1.12 mL
D.阴极的电极反应式是2HSO3-+2H++2e-= S2O42-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是( )

A.反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B.乙装置中铁电极为阴极,电极反应式为Fe-2e-=Fe2+
C.甲中通入氧气的一极为阳极,发生的电极反应为O2+4e-+2H2O=4OH-
D.反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。常温时,H2S在水中的电离常数Ka1=1.3×10-7,Ka2=7.0×10-15。按要求回答下列问题:
(1)H2S在水中的二级电离常数表达式Ka2=______;0.1mol/LNa2S溶液中离子浓度由大到小的顺序为__________.
(2)常温下,向0.1mol/LH2S溶液中通入HCl或加入NaOH固体,测得c(S2-)与溶液pH的关系如图(忽略溶液体积的变化及H2S的挥发)。

①当溶液中c(S2-)=1.4×10-19mol/L时,溶液中c(OH-)=______,水电离产生的c(H+)=______.
②当pH=13时,溶液中的c(H2S)+c(HS-)=_______.
(3)在工业废水处理中常用H2S将Mn2+转化为MnS除去。常温下,向含有0.010mol·L-1 Mn2+废水中通入H2S以调节废水的pH,当c(HS-)=2.0×10-4mol·L-1时,Mn2+开始沉淀,此时废水的pH=___。[已知Ksp(MnS)=1.4×10-15]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
A. v(N2)=0.25 mol·L-1·min-1
B. v(H2)=0.75 mol·L-1·min-1
C. v(NH3)=1 mol·L-1·min-1
D. v(NH3)=0.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是

A. K与N连接时,X为硫酸,一段时间后溶液的pH增大
B. K与N连接时,X为氯化钠,石墨电极反应:2H++2e-=H2↑
C. K与M连接时,X为硫酸,一段时间后溶液的pH增大
D. K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-=2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为﹣2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是

A. 晶体中每个K+周围有8个O2﹣,每个O2﹣周围有8个K+
B. 晶体中与每个K+距离最近的K+有8个
C. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2﹣
D. 晶体中,0价氧与﹣2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系中共有KCl、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 七种物质:
七种物质:
(1)写出一个包含上述七种物质的氧化还原反应方程式:____________。
(2)上述反应中,1mol氧化剂在反应中得到________mol电子。
(3)如果在反应后的溶液中加入![]() ,溶液又变紫红色。已知铋有
,溶液又变紫红色。已知铋有![]() 、
、![]() 价,其中
价,其中![]() 价较稳定,写出加入
价较稳定,写出加入![]() 溶液又变紫红色的离子方程式:_________。由上述方程式说明
溶液又变紫红色的离子方程式:_________。由上述方程式说明![]() 的一个性质:__________。
的一个性质:__________。
II.(1)已知![]() 能与次氯酸盐发生如下反应(未配平)
能与次氯酸盐发生如下反应(未配平)![]() 。
。
①已知有10.7gFe(OH)3参加反应,共转移了![]() 个电子,则
个电子,则![]() ________。
________。
②根据所学的知识,推测![]() 能和下列________
能和下列________![]() 填序号
填序号![]() 物质反应。
物质反应。
A.![]() B.SO2 C.
B.SO2 C.![]() D.
D.![]()
(2)一定条件下,向含硝酸的废水中加入![]() ,将
,将![]() 还原成
还原成![]() 。若该反应消耗32gCH3OH,转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
。若该反应消耗32gCH3OH,转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com