
| A. | 向Ba(0H)2溶液中滴H2SO4溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 明矾溶液中加氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba+4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| D. | 向100mL0.1mol/L的FeBr2溶液中通入0.012molCl2:10Fe2++14Br-+12Cl2═10Fe3++7Br2+24Cl- |
分析 A.至中性,生成硫酸钡和水,不符合离子的配比;
B.产生沉淀的物质的量达最大值,生成硫酸钡、氢氧化铝和水;
C.反应生成碳酸钙、氢氧化镁;
D.n(FeBr2)=0.01mol,通入0.012molCl2,由电子守恒可知,亚铁离子全部被氧化,溴离子部分被氧化.
解答 解:A.向Ba(0H)2溶液中滴H2SO4溶液至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故A错误;
B.明矾溶液中加氢氧化钡溶液,使其产生沉淀的物质的量达最大值的离子反应为22Al3++3SO42-+3Ba+6OH-═3BaSO4↓+2Al(OH)2↓,故B错误;
C.Mg(HCO3)2溶液中加入过量石灰水的离子反应为Mg2++2HCO3-+Ca2++4OH-═CaCO3↓+2H2O+Mg(OH)2↓,故C错误;
D.n(FeBr2)=0.01mol,通入0.012molCl2,由电子守恒可知,亚铁离子全部被氧化,溴离子部分被氧化,则离子反应为10Fe2++14Br-+12Cl2═10Fe3++7Br2+24Cl-,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 洗涤沉淀时,应用玻璃棒轻轻搅拌,使得沉淀表面上的杂质溶于水中 | |
| B. | 将两块未擦去氧化膜的铝片分别投入1mol?L-1CuSO4溶液、1mol?L-1CuCl2溶液中,一段时间后,铝片表面都观察不到明显的反应现象 | |
| C. | 由锌、铜、稀硫酸构成的原电池溶液中加入适量的H2O2能提高电池的放电效率 | |
| D. | 在淀粉溶液中加入适量稀硫酸微热,再加少量新制氢氧化铜浊液加热,若无砖红色沉淀产生,则淀粉未发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水褪色;乙醇使高锰酸钾溶液褪色 | |
| B. | 油脂的皂化反应;乙烯制乙醇 | |
| C. | 蔗糖水解;乙醇和乙酸制乙酸乙酯 | |
| D. | 苯制溴苯;苯和氢气制环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
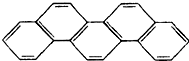 有一种有机物,因其酷似奥林匹克五环旗(如图),科学家称其为“奥林匹克烃”,下列有关“奥林匹克烃”的说法正确的是( )
有一种有机物,因其酷似奥林匹克五环旗(如图),科学家称其为“奥林匹克烃”,下列有关“奥林匹克烃”的说法正确的是( )| A. | 该有机物属芳香烃 | |
| B. | 该物质属氨基酸 | |
| C. | 该物质分子中只含非极性键 | |
| D. | 该物质完全燃烧产生水的物质的量小于CO2的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CuSO4溶液中的Fe(SO4)3,加入足量CuO粉末,充分搅拌过滤 | |
| B. | 烧碱、小苏打、氢氧化铝均可用于治疗胃酸过多 | |
| C. | 工业生产中,常将氯气通入澄清石灰水中,制取漂白粉 | |
| D. | 铁管道与直流电源正极相连,可缓解管道腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中含有碳碳三键的不饱和链烃 | |
| B. | 易发生加成反应 | |
| C. | 既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 | |
| D. | 分子里所有的碳原子都处于同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2通入酸化的KI淀粉溶液中 | |
| B. | CO2通入CaCl2溶液中 | |
| C. | 0.1mol•L-l稀H2SO4滴入0.1 mol•L-1Na2S2O3溶液中 | |
| D. | 0.2mol•L-1H2C2O4溶液滴入酸化的KMnO4溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com