
����Ŀ����Ȳ���ڴ��������¿ɷ���ż����Ӧ����ΪGlaser��Ӧ��2R-C��C-H![]() R-C��C-C��C-R+H2, �÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�
R-C��C-C��C-R+H2, �÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�

�ش��������⣺
(1)B�Ľṹ��ʽΪ________��D�Ļ�ѧ����Ϊ________��
(2)�ٺ͢۵ķ�Ӧ���ͷֱ�Ϊ________��________��
(3)E�Ľṹ��ʽΪ______����1 mol E�ϳ�1,4���������飬��������Ҫ��������__ mol��
(4)������(![]() )Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ__________��
)Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ__________��
(5)���㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3��1��д������3�ֵĽṹ��ʽ_____________________________________________��
���𰸡�![]() ����Ȳ ȡ����Ӧ ��ȥ��Ӧ
����Ȳ ȡ����Ӧ ��ȥ��Ӧ ![]() 4 n
4 n![]()
![]()
![]() +nH2O
+nH2O 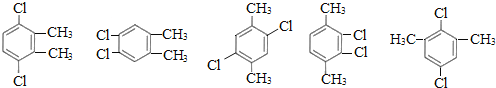
��������
��1��A�������鷢��ȡ����Ӧ����B�������B����ʽ��֪A�DZ���B�DZ����飬��B�Ľṹ��ʽΪ![]() ������D�Ľṹ��ʽ
������D�Ľṹ��ʽ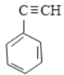 ��֪D �Ļ�ѧ����Ϊ����Ȳ��
��֪D �Ļ�ѧ����Ϊ����Ȳ��
��2�����DZ�������ԭ�ӱ��һ�ȡ��������ȡ����Ӧ�����в���̼̼��������±��������ȥ��Ӧ��
��3��D������֪��Ϣ�ķ�Ӧ�����E�Ľṹ��ʽΪ![]() ��1��̼̼������Ҫ2���������ӳɣ�����1 mol E�ϳ�1��4�����������飬��������Ҫ��������4mol��
��1��̼̼������Ҫ2���������ӳɣ�����1 mol E�ϳ�1��4�����������飬��������Ҫ��������4mol��
��4��������֪��Ϣ��֪�����![]() ������Glaserż����Ӧ���ɾۺ���Ļ�ѧ����ʽΪn
������Glaserż����Ӧ���ɾۺ���Ļ�ѧ����ʽΪn![]()
![]()
![]() +nH2O��
+nH2O��
��5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1��������������л���ṹ��ʽΪ ��
��


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����а���(��NH2)�Ļ�����ͨ���ܹ������ᷴӦ�����������Σ��磺R��NH2��HCl�D��R��NH2��HCl(R���������������)��
�������ֻ�����A��B�����ǻ�Ϊͬ���칹�塣��֪��
�����Ƕ��Ƕ�λ��ȡ������
�����ǵ���Է�����������137��
��A���ܱ�NaOH��Һ�кͣ��ֿ��Ը�������Σ���������FeCl3��Һ������ɫ��Ӧ��B�Ȳ��ܱ�NaOH��Һ�кͣ�Ҳ���ܸ�������Σ�
�����ǵ����Ԫ��ֻ������C��H��O��N��Cl�еļ��֡�
�밴Ҫ����գ�
(1)A��B�ķ���ʽ��________________��
(2)A�Ľṹ��ʽ��_____________________________��
B�Ľṹ��ʽ��______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����̿�(��Ҫ�ɷ�ΪMnO2)�������Ʊ��̼��仯����ִ�ұ�������̵Ĺ�����������ͼ��ʾ������������������һ������

�±�Ϊt��ʱ���й����ʵ�Ksp
���� | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
Ksp | 4.0��10-38 | 2.2 | 5.5 | 1.9 | 6.3 | 9.1 | 2.5 | 2.2 |
���̿�ԭ�����ķ�ӦΪ��12MnO2��C6H12O6��12H2SO4===12MnSO4��6CO2����18H2O
��1��д��һ�������ԭ�������ʵĴ�ʩ��_________________________
��2������pH ���������ɵij���Ϊ________������MnF2����ҪĿ���dz�ȥ__________ (�Ca2��������Fe3������Cu2����)
��3����Ũ�ȵģ�NH4)2S�루N4)2SO4 ��Һ�У�NH4����Ũ�ȴ�СΪ��ǰ��________���ߣ������������ �� ��=�� )��
��4����MnSO4��ȡMnCO3��MnSO4��Һ�м���(NH4)2CO3��Һ����MnCO3��ͬʱ�������Mn(OH)2�����ܵ�ԭ���У�MnCO3(s)��2OH��(aq)![]() Mn(OH)2(s)��CO
Mn(OH)2(s)��CO![]() (aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K��_________________(����һλС��)��
(aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K��_________________(����һλС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��������������ȷ����(����)
A.����C��H��O����Ԫ�ص��л��������
B.�������ʾ�����������Һ�ڼ���ʱ������Ӧ��������
C.�������ʶ�����ζ
D.������������ɫֲ�������õIJ���Ƕ�ֲ��������������Ҫ��Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���ѧ����������ᡢ����������أ����������в���ȷ���ǣ� ��
A.�����������˱ȳ���������
B.����й©��Ӧ˳����ʹ���
C.����ȼúʹ�ã������ڽ��Ϳ�����PM2.5����
D.��������Ͷ�����������Ҫ�Ĵ�����Ⱦ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
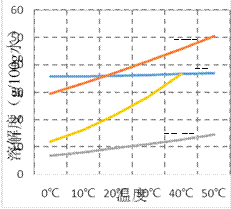
����Ŀ��CaCO3��ϡ���ᷴӦ����CO2�����뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�����н�������ȷ����
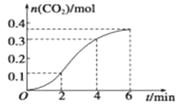
A. ��Ӧ��2��4 min��ƽ����Ӧ�������
B. ��Ӧ��ʼ4 min���¶ȱ�Ũ�ȶԷ�Ӧ���ʵ�Ӱ���
C. 4 min��Ӧ���ʼ�С����Ҫԭ����c(H��)��С
D. ��Ӧ��2��4 min������CO2��ƽ����Ӧ����Ϊv(CO2)��0.1 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�ֵ���ɫ���壬�����������̼��Ӧ������������DZˮͧ�����������������������֮�á����������̼��Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2��ijѧ��Ϊ����֤��һʵ�飬�������Ĵ���ʯ�������������1.95g����������ƷΪԭ�ϣ���ȡO2����Ƴ�����ʵ��װ�ã�
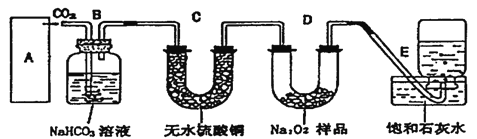
��l��A����ȡCO2��װ�ã�Ӧ������ͼ������������ѡ�ĸ�ͼ��_____��
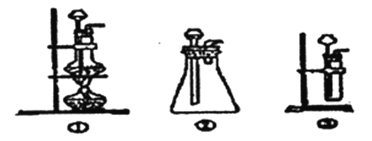
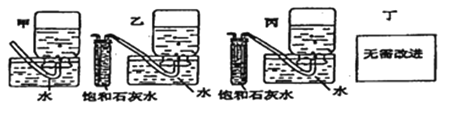
Bװ�õ�������________, Cװ���ڿ��ܳ��ֵ�������________��Ϊ�˼���E���ռ��������壬��ȡ������ƿ����________��ľ�����뼯��ƿ�ڣ�ľ�������________��
��2����E�е�ʯ��ˮ��������ɫ���ǣ���˵��ԭ��________��
��3����D�е�1.95g����������Ʒ�ӽ���Ӧ���ʱ����Ԥ��Eװ�����к�����________��
��4����Ӧ���ʱ�������E�еļ���ƿ�ռ���������Ϊ250mL����֪�������ܶ�Ϊ1.43g/L����װ�õ����������õ�����£�ʵ���ռ�����������������ۼ���ֵ______������С�������Լ________mL��ȡ����ֵ���������ݾ��ڱ�״���²ⶨ������������________��
��5������Ϊ����A��E��ʵ��װ���У�E�����Ƿ�ȫ��������E�Ƿ���Ҫ��Ϊ���������е���һ�________�����üס��ҡ��������ش�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ȡ�����������������ͼ��ʾ��
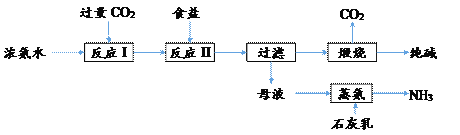
���������գ�
��1��Nԭ�Ӻ�����_______�ֲ�ͬ�˶�״̬�ĵ��ӣ��������������Ų�ʽ��________����ɴ����Ԫ��ԭ�Ӱ뾶�Ӵ�С����Ϊ___________________��
��2����ˮ�dz��õ��ʣ��ð�ˮʩ��ʱҪ�ܿ����¡����������ԭ����_______________��
��3�������ӷ���ʽ��ʾ̼���Ʊ���Ϊ�����ԭ��_____________________________ ��
��4�������ͼ���ܽ�ƽ�����۽��ͷ�ӦII�ķ�Ӧԭ��____________________________________��
��5������ĸҺ��ͨ��ʯ�����������֮ǰ��ͨ����Ҫ�Ƚ�ĸҺ���ȡ��������ȣ�����ʯ�������ײ������������ܵ������ɵij�����________��
��6�����������п���ѭ�����õ�������________����������______________��
��7�����û���������ѭ��һ��ԭ��������������������̣�ָ������֮��____________________��дһ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Ϊ���ۺ��������������еĸ���ƷCaSO4�������ڵĺϳɰ�����������������Ʊ�(NH4)22SO4�Ĺ������̣�
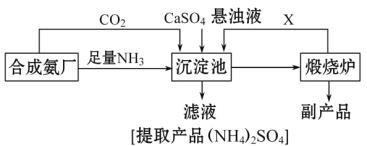
��ش��������⣺
��1����ҵ�ϳɰ���Ӧ��������_____________________���������з�������Ҫ��Ӧ����ʽ��________________________���÷�Ӧ�ܹ�������ԭ����__________________________��
��2���ᴿ��Һ�Ի��(NH4)2SO4���壬��Ҫ�IJ��������ǣ�__________������ţ���
A����ȡ B������Ũ�� C����ȴ�ᾧ D������
��3���������������У��й�NH3�����ü�˵����ȷ���ǣ�__________������ţ���
A���ṩ�Ʊ�����ĵ�Ԫ��
B������CO32-��Ũ�ȴٽ���Ӧ����
C������Ӧ�Ĵ���
D������1 mol (NH4)2SO4����������2 mol NH3
��4�������������еĸ���Ʒ��_______________������ɫ��ѧ����Դ�ۺ����õĽǶ�˵���������̵���Ҫ�ŵ���______________.ȱ����_____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com